Comptes rendus
D’après Arthritis Rheum 2012;64(12):3850-5; Arthritis Rheum 2013:65(1):28-38; The Lancet publié en ligne le 18 mars 2013.
Le présent compte rendu est fondé sur des données médicales présentées lors d'un congrès de médecine reconnu ou publiées dans une revue avec comité de lecture ou dans un commentaire signé par un professionnel de la santé reconnu. La matière abordée dans ce compte rendu s'adresse uniquement aux professionnels de la santé reconnus du Canada.
MEDI-NEWS - Comparaisons directes d’agents biologiques dans la polyarthrite rhumatoïde : pour en avoir le cœur net
Mars 2013
Depuis une dizaine d’années, les agents biologiques améliorent significativement la prise en charge des patients atteints de polyarthrite rhumatoïde (PR), et la tendance se poursuit avec l’avènement d’agents biologiques aux modes d’action variés. Jusqu’à tout récemment, les agents biologiques n’avaient jamais fait l’objet d’une comparaison directe, et la sélection d’un agent pour le traitement de la PR était plutôt arbitraire compte tenu de l’absence de données comparatives. Cependant, l’efficacité clinique et l’innocuité de divers agents biologiques ont fait l’objet de trois études comparatives à court et à long terme dont les résultats ont été publiés. Bien qu’il ne soit pas possible de trancher sur la supériorité d’un agent biologique par rapport aux autres à la lumière de ces études comparatives, les résultats devraient faciliter la sélection d’un traitement tenant compte de la sévérité de la maladie et des préférences personnelles.
Rédactrice médicale en chef : Dre Léna Coïc, Montréal, Québec
Monothérapie : inhibition de l’IL-6 vs inhibition du TNF
Parmi les essais comparatifs directs sur les agents biologiques dont les résultats ont été publiés, l’essai ADACTA est le plus récent. Comme environ le tiers des patients atteints de polyarthrite rhumatoïde (PR) reçoivent un agent unique, il est important d’évaluer l’efficacité des agents biologiques en monothérapie. Dans cette étude, le tocilizumab seul a été comparé à l’adalimumab seul (Lancet 2013;publié en ligne avant impression, 18 mars).
Les 326 sujets de l’essai ADACTA étaient atteints de PR sévère au départ et ne toléraient pas leur traitement par le méthotrexate (MTX) ou ne pouvaient plus le poursuivre. La moitié de la cohorte recevait 8 mg/kg de tocilizumab par voie intraveineuse (i.v.) toutes les 4 semaines alors que l’autre recevait 40 mg d’adalimumab par voie sous-cutanée (s.c.) toutes les 2 semaines.
Fait digne de mention, cet essai a été le premier à évaluer la supériorité d’un agent biologique par rapport à un autre, et il a révélé que les taux de réponse étaient significativement supérieurs pour tous les paramètres, tant primaire que secondaires.
Contrairement à l›adalimumab, inhibiteur du facteur de nécrose tumorale (anti-TNF), le tocilizumab se lie à la fois aux récepteurs membranaires et solubles de l’interleukine-6 (IL-6) humaine, inhibant ainsi la signalisation relevant de l’IL-6 et ses effets inflammatoires.
Le paramètre principal de l’étude était la variation de l’activité de la maladie entre le début de l’étude et la 24e semaine telle qu’évaluée par le score DAS28 (Disease Activity Score pour 28 articulations). Lorsqu’on évalue l’efficacité clinique à 24 semaines, il faut garder à l’esprit que les sujets de l’essai ADACTA avaient un score DAS28 élevé (>5,1) au départ. Le pourcentage de sujets ayant atteint les critères de l’American College of Rheumatology ACR50 et ACR70 était significativement plus élevé sous tocilizumab (47 % et 33 %, respectivement) que sous adalimumab (28 % et 18 %).
Comme le soulignent les auteurs, le nombre absolu moyen d’articulations gonflées et sensibles au toucher a diminué avec le temps dans les deux groupes, mais les diminutions étaient plus fréquentes dans le groupe recevant l’inhibiteur de l’IL-6. La proportion de patients dont le nombre d’articulations gonflées était de zéro à 24 semaines était semblable dans les deux groupes : 38 % sous tocilizumab et 30 % sous adalimumab.
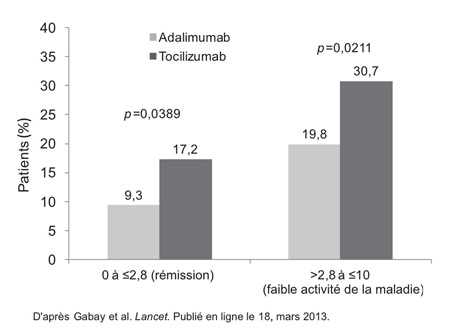
Toujours à 24 semaines, les patients recevant l’inhibiteur de l’IL-6 étaient aussi plus nombreux que les patients recevant l’anti-TNF à être parvenus à la rémission selon l’indice CDAI (Clinical Disease Activity Index) : 17,2 % vs 9,3 %; p<0,0389 (Figure 1). À partir de la 16e semaine, les patients sous tocilizumab ont été plus nombreux que les patients sous adalimumab à atteindre la rémission selon les critères de l’ACR et de l’EULAR, si bien qu’à 24 semaines, 18,4 % des patients sous tocilizumab étaient en rémission selon les critères ACR/EULAR vs 11,1 % des patients sous adalimumab (p=0,0569).
L’incidence des effets indésirables (EI) était également comparable dans les deux groupes, mais les modifications de dose et interruptions du traitement motivées par des EI ont été plus fréquentes sous tocilizumab (24,7 %) que sous adalimumab (18,5 %). Les EI les plus fréquents étaient les infections et les infestations, généralement légères à modérées, et les infections graves ont été rares dans les deux groupes.
Figure 1. ADACTA : indice CDAI à 24 semaines (analyse en IT)
Comparaison d’un anti-TNF et d’un modulateur des lymphocytes T
L’essai AMPLE (Abatacept versus Adalimumab Comparison in Biologic-Naive RA Subjects with Background Methotrexate) visait à comparer l’abatacept, un modulateur des lymphocytes T, à raison de 125 mg/semaine par voie s.c. avec l’adalimumab, un anti-TNF, à raison de 40 mg toutes les 2 semaines, par voie s.c., tous deux en association avec le MTX (Arthritis Rheum 2013:65[1]:28-38). Le score moyen DAS28-CRP était de 5,5 au départ, et la proportion de patients dont la maladie était modérément ou très active était identique dans chaque groupe. Au total, 646 patients ont été randomisés, et la majorité d’entre eux ont été traités pendant la totalité des 12 mois.
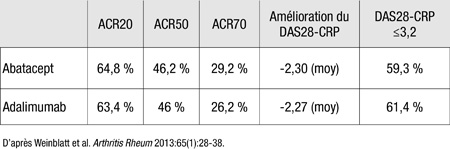
Le paramètre principal était la non-infériorité de l’un par rapport à l’autre selon le pourcentage de patients ayant atteint le critère ACR20 à 1 an. Les taux de réponse après 1 an de suivi étaient semblables (Tableau 1).
Tableau 1. AMPLE : Résultats à 1 an
Comme l’indiquent les auteurs, la proportion de patients en rémission était comparable dans les deux groupes de traitement, sans égard à l’indice utilisé pour mesurer la rémission. Selon les critères ACR/EULAR, les taux de rémission étaient aussi semblables : 13,5 % sous abatacept vs 15,7 % sous adalimumab.
L’évaluation de l’atteinte radiographique, paramètre qui «signe» un essai sur la PR digne de ce nom, a généré des données objectives et quantifiables. Dans cette étude, les données radiographiques ont fait ressortir des améliorations «similaires et robustes» des scores d’érosion et de pincement de l’interligne articulaire dans les deux groupes. Sur le plan de l’innocuité, les résultats étaient comparables dans les deux groupes pour la plupart des paramètres; les EI graves n’ont pas fait exception, le taux ayant été d’environ 10 % dans chaque groupe.
Comparaison d’anti-TNF
Deux anti-TNF, l’étanercept et l’adalimumab, ont fait l’objet d’une autre étude comparative directe sur l’issue clinique à long terme dont les résultats ont été publiés récemment, et les auteurs ont porté une attention particulière à la réponse au traitement chez les patients qui développaient des anticorps anti-adalimumab (Arthritis Rheum 2012;64[12]:3850-5). Les sujets de l’étude, qui n’avaient jamais été exposés à un anti-TNF, ont été randomisés de façon à recevoir de l’étanercept à raison de 50 mg/semaine par voie s.c. ou de 25 mg 2 fois/semaine par voie s.c. (n=203) ou de l’adalimumab à raison de 40 mg toutes les 2 semaines par voie s.c. (n=204). L’objectif clinique était l’obtention et le maintien durable (≥12 mois consécutifs) d’une faible activité de la maladie telle que mesurée par un score DAS28 à <3,2, d’une activité minime de la maladie (DAS28 <2,6) ou d’une rémission ACR/EULAR selon l’indice SDAI (Simplified Disease Activity Index).
Au départ, la maladie était active (DAS28 ≥3,2) malgré l’administration antérieure d’au moins deux agents de rémission traditionnels (DMARD), y compris le MTX. Au total, 58 % des patients sous adalimumab et 55 % des patients sous étanercept ont reçu le traitement pendant 3 ans. Le traitement par l’adalimumab a duré 143 semaines (médiane) et le traitement par l’étanercept, 130 semaines (médiane). Après 3 ans de suivi, les taux de réponse clinique étaient similaires (Tableau 2).
Tableau 2.
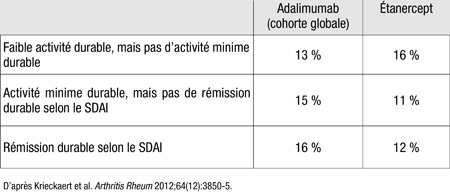
Il importe ici de souligner que plus du quart des patients sous adalimumab ont développé des anticorps anti-adalimumab durant le traitement et que, chez ces patients, la réponse au traitement était considérablement plus faible : seulement 13 % des patients ont atteint le critère «faible activité durable, mais pas d’activité minime durable»; aucun patient n’est parvenu au critère «activité minime durable, mais pas de rémission durable selon le SDAI»; et seulement 4 % des patients ont obtenu une rémission durable selon le SDAI. Les pourcentages correspondants pour les patients qui n’avaient pas développé d’anticorps contre l’adalimumab étaient de 13 %, 20 % et 20 %, respectivement. Fait peut-être digne de mention, le risque d’apparition de tels anticorps était plus élevé chez les patients dont la maladie était sévère depuis longtemps et chez ceux qui ne recevaient pas de traitement concomitant par un DMARD. Dans le traitement de la PR chez des patients jamais exposés à un anti-TNF, l’adalimumab et l’étanercept sont d’efficacité similaire, concluent les auteurs.
Cela dit, les auteurs estiment que si une très petite proportion de patients jamais exposés à un anti-TNF a atteint la rémission dans cette étude, c’est dire qu’il y a place à l’amélioration sur le plan de l’efficacité de ces agents biologiques coûteux.
Résumé
Jusqu’à maintenant, la sélection d’un agent biologique demeurait empirique, car peu d’études avaient comparé des agents biologiques. Pour la première fois, il a été démontré que le tocilizumab était supérieur à un anti-TNF en monothérapie, ce qui donne tout lieu de croire que l’interruption de la voie IL-6 de l’inflammation contribue étroitement à la maîtrise de la PR. Pris collectivement, les résultats de ces essais comparatifs s’ajoutent à d’autres données qui permettront de faire des choix éclairés tenant compte de la sévérité de la PR et des préférences personnelles.