Comptes rendus
Retombées de l'inhibition de l'IL-17A sur la sévérité de la maladie et les changements structuraux dans la spondylarthrite axiale
Le présent compte rendu est fondé sur des données médicales présentées lors d'un congrès de médecine reconnu ou publiées dans une revue avec comité de lecture ou dans un commentaire signé par un professionnel de la santé reconnu. La matière abordée dans ce compte rendu s'adresse uniquement aux professionnels de la santé reconnus du Canada.
FRONTIERES MEDICALES - l’assemblée annuelle de l’American College of Rheumatology
San Diego, Californie / 4-7 novembre 2017
San Diego – Le traitement de la spondylarthrite axiale (SAax) – qui englobe l’arthrite psoriasique et la spondylarthrite ankylosante – cible à la fois les symptômes articulaires et les lésions articulaires structurales. L’inhibition de l’interleukine-17A, cytokine majeure intervenant dans la pathogenèse de la SAax, atténue les symptômes de la maladie tout en ralentissant sa progression radiographique. De récents résultats indiquent que les améliorations se maintiennent à 4 ans.
Rédactrice médicale en chef : Dre Léna Coïc, Montréal, Québec
Au déclin de la capacité fonctionnelle associé à l’arthrite psoriasique (AP) et à la spondylarthrite ankylosante (SA) s’ajoutent des lésions structurales érosives qui influent aussi sur la capacité fonctionnelle et la mobilité rachidienne. Ainsi, les traitements qui ralentissent la progression de l’atteinte articulaire structurale pourraient offrir des avantages autres qu’une diminution de l’intensité des douleurs et des raideurs articulaires. Selon des données, en plus d’atténuer les signes et les symptômes de la SA et de l’AP, les inhibiteurs de l’interleukine (IL)-17A inhiberaient la progression des lésions structurales articulaires.
Faible progression radiographique de la SA à 4 ans
Dans la SA, la progression structurale – qui se caractérise par une néoformation osseuse – peut mener à l’ankylose des articulations sacro-iliaques (ASI) et du rachis. Les traitements de fond qui peuvent ralentir la progression structurale comblent un vide, affirme le Dr Jürgen Braun, directeur médical, Rheumazentrum Ruhrgebiet, Herne, Allemagne.
Dans MEASURE 1, l’atténuation des signes et des symptômes de la SA se maintenait à 2 ans sous sécukinumab, anticorps monoclonal anti-IL-17A entièrement humain. De plus, aucune progression radiographique n’était visible chez environ 80 % des patients.
«Cette étude a prouvé l’efficacité de la dose [homologuée] de 150 mg pendant 4 ans, poursuit le Dr Braun. Il n’y a eu aucune progression chez la majorité des patients.»
Les résultats de la prolongation de MEASURE 1 appuient l’effet durable du sécukinumab sur les symptômes et la progression radiographique à 4 ans (208 semaines). Au total, 371 patients atteints de SA évolutive ont reçu aléatoirement 10 mg/kg de sécukinumab ou un placebo par voie i.v. à 0, 2, et 4 semaines, puis 150 mg ou 75 mg ou un placebo par voie s.c. toutes les 4 semaines à partir de la semaine 8. Les patients sous placebo répondant aux critères de réponse ASAS (Assessment of Spondyloarthritis International Society) 20 à 16 semaines passaient au sécukinumab à 24 semaines. Les non-répondeurs recevaient 75 mg ou 150 mg de sécukinumab à 16 semaines, puis toutes les 4 semaines.
Des radiographies de profil des rachis cervical et lombaire effectuées au départ, puis à 104 et 208 semaines permettaient de mesurer la progression radiographique. Le lecteur – un seul par patient – établissait le score mSASSS (modified Stoke Ankylosing Spondylitis Spine Score) à partir des images numérisées.
À 3 ans, 79,5 % et 60,9 % des patients sous sécukinumab (150 mg) avaient une réponse ASAS20 et ASAS40, respectivement. Depuis le début de l’étude, l’indice BASDAI (Bath Ankylosing Spondylitis Disease Activity Index) avait varié en moyenne de -3,1; l’indice BASFI (Bath Ankylosing Spondylitis Functional Index), de -2,8; et l’indice BASMI (Bath Ankylosing Spondylitis Metrology Index), de -0,7; toutes les variations s’apparentaient à celles observées à 2 ans.
À 4 ans, 79,7 % avaient une réponse ASAS20 et 60,8 %, une réponse ASAS40 (cas observés) – «bref, une réponse clinique durable au sécukinumab», enchaîne le Dr Braun. À 208 semaines, la variation d’activité par rapport au début de la maladie était de -3,4 selon l’indice BASDAI, de -2,9 selon l’indice BASFI, et de -0,5 selon l’indice BASMI.
À 2 ans, le score mSASSS moyen avait varié de 0,30 (toutes doses confondues). Selon ce score, la progression demeurait faible à 4 ans. Chez les patients recevant 150 mg, la variation moyenne à 4 ans était de 1,2, et comparativement à ceux qui recevaient 75 mg, la progression était plus lente. Cette étude comparative sur un agent biologique dans la SA est la première à faire ressortir un lien entre la dose et l’ampleur de l’inhibition de la progression structurale, note le Dr Braun. À 4 ans, quelque 78,9 % des patients sous sécukinumab ne montraient aucune progression radiographique (variation du score mSASSS <2 par rapport au score initial) (Figure 1).
En 4 ans, un effet indésirable avait motivé l’arrêt du traitement chez 32 (8,9 %) des 360 patients. Parmi les effets indésirables graves figuraient 21 cas d’uvéite (antécédents dans 4 cas), 7 cas de maladie de Crohn (antécédents dans 2 cas) et 2 cas de colite ulcéreuse.
Figure 1.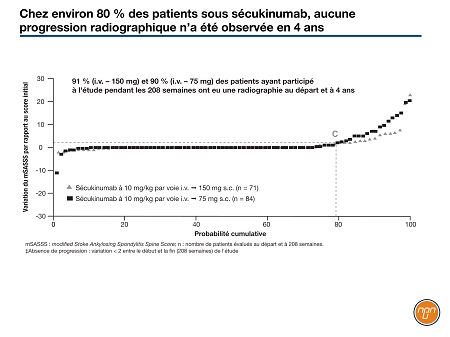
Effet sur l’atteinte structurale associée à l’AP
Le traitement par le sécukinumab, surtout si amorcé avec une dose d’attaque, a inhibé la progression radiographique de l’atteinte articulaire structurale chez les patients atteints d’AP.
Dans FUTURE 5, à 24 semaines, les patients sous sécukinumab étaient significativement plus nombreux que les patients sous placebo à ne montrer aucune aggravation de l’atteinte articulaire structurale, affirme le Dr Philip J. Mease, directeur, recherche clinique en rhumatologie, University of Washington, Seattle, États-Unis. Le profil d’innocuité du sécukinumab était conforme au profil connu, aucun nouveau problème n’ayant été signalé.
Le sécukinumab est le deuxième anti-IL-17A à inhiber la progression radiographique dans l’AP. Dans l’essai SPIRIT-P1 – dont le Dr Mease était aussi le chercheur principal –, l’ixékizumab s’était révélé supérieur au placebo et à l’adalimumab quant à la progression de l’atteinte structurale chez les patients atteints d’AP n’ayant jamais reçu d’agent biologique. La population de FUTURE 5 incluait à la fois des patients n’ayant jamais reçu d’anti-TNF (facteur de nécrose tumorale) et des patients n’ayant pas répondu adéquatement à un anti-TNF.
Deux anti-IL-17A qui inhibent l’atteinte structurale de l’AP, «c’est rassurant, explique le Dr Mease. À long terme, nous pouvons aspirer à l’inhibition de la progression radiographique.»
Dans FUTURE 5, 996 adultes atteints d’AP évolutive ont reçu aléatoirement : 300 mg de sécukinumab avec dose d’attaque de 300 mg; 150 mg de sécukinumab avec ou sans dose d’attaque de 150 mg; ou un placebo. Tous les groupes ont reçu du sécukinumab ou un placebo au départ, à 1, 2, 3 et 4 semaines, puis toutes les 4 semaines.
Une amélioration ≥20 % du score ACR à 16 semaines par rapport au score initial (paramètre principal) a été observée chez 62,6 % des patients du groupe 300 mg + dose d’attaque, comparativement à 27,4 % des patients sous placebo (p<0,0001). Quelque 55,5 % des patients du groupe 150 mg + dose d’attaque et 59,5 % du groupe 150 mg sans dose d’attaque sont parvenus à une réponse ACR20 (p<0,0001 pour les deux groupes de 150 mg).
La variation du score vdH-mTSS (van der Heijde-modified Total Sharp Score) moyen par rapport au score initial déterminait la progression radiographique de l’atteinte structurale. À 24 semaines, 88 % des patients du groupe 300 mg ne montraient aucune progression radiographique, vs 80 % des patients du groupe 150 mg + dose d’attaque, 84 % du groupe 150 mg sans dose d’attaque, et 74 % des patients sous placebo.
À 24 semaines, au sein de la population totale, le score vdH-mTSS (Figure 2) avait varié en moyenne de 0,5 sous placebo, de 0,08 dans le groupe 300 mg (p<0,01), de 0,17 dans le groupe 150 mg avec dose d’attaque (p<0,05 vs placebo) et de -0,09 dans le groupe 150 mg sans dose d’attaque (p<0,01 vs placebo). Chez les patients n’ayant jamais reçu d’anti-TNF, le score vdH-mTSS avait varié de 0,48 sous placebo, de 0,01 dans le groupe 300 mg (p<0,001), de 0,12 dans le groupe 150 mg avec dose d’attaque (p<0,05 vs placebo) et de -0,25 dans le groupe 150 mg sans dose d’attaque (p<0,05 vs placebo).
Figure 2.
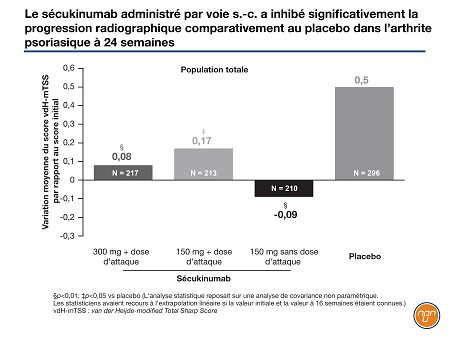
L’enthésite s’est résorbée chez 61,4 % des patients du groupe 300 mg, et la différence par rapport au groupe placebo (34,4 %) était significative (p<0,0001). La différence entre les groupes 150 mg avec (p<0,05) et sans (p<0,001) dose d’attaque et le groupe placebo était également significative. La résorption complète de la dactylite était aussi significativement plus fréquente sous sécukinumab que sous placebo (p<0,0001 pour tous les groupes sécukinumab).
«À en juger par ces données, il faudrait idéalement prescrire 300 mg de sécukinumab avec une dose d’attaque : 5 injections initiales suivies de 1 injection mensuelle», conclut-il.
La DreDésirée van der Heijde, professeure de rhumatologie, Centre médical de l’Université de Leyde, Pays-Bas, a présenté des données à 52 semaines sur la progression radiographique de l’atteinte articulaire structurale associée à l’AP évolutive. Les 417 sujets de cette étude de phase III à double insu ont reçu aléatoirement pendant 24 semaines soit une dose d’attaque de 160 mg d’ixékizumab, puis 80 mg toutes les 2 ou 4 semaines, soit un placebo, soit 40 mg d’adalimumab toutes les 2 semaines. Lors de la prolongation, 381 patients initialement sous placebo ou adalimumab ont été randomisés de nouveau : ixékizumab toutes les 2 ou 4 semaines. L’atteinte articulaire structurale était évaluée par le score vdH-mTSS.
À 52 semaines, le score avait varié en moyenne de 0,54 et de 0,09 chez les patients randomisés au départ dans les groupes ixékizumab toutes les 4 semaines et toutes les 2 semaines, respectivement. Chez la plupart de ces patients, il n’y avait aucune progression de l’atteinte structurale à 1 an.
Prédicteurs de l’atteinte structurale et réponse au traitement
Des chercheurs de l’Université de Leyde ont constaté qu’une inflammation locale de l’ASI et du rachis détectée à l’IRM chez des patients atteints de SAax débutante était associée après 5 ans à l’apparition d’une atteinte structurale à l’IRM. Dans leur étude, 155 patients atteints de SAax datant de 3 ans ou moins ont passé une IRM au départ et à 5 ans. La présence d’un œdème de la moelle osseuse de l’ASI et du rachis au départ était un solide prédicteur de la présence d’au moins 3 lésions graisseuses dans les 2 localisations 5 ans plus tard. La survenue de lésions graisseuses (progression structurale nette) était ainsi plus probable chez les patients présentant au départ un œdème médullaire au niveau de l’ASI que chez les patients n’en présentant pas. L’effet était indépendant de l’inflammation systémique mesurée par le taux de protéine C-réactive ultrasensible.
Dans l’étude de phase III ASTREA sur l’AP, l’équipe du Dr Georg Schett, professeur et directeur du département de médecine, de rhumatologie et d’immunologie, Université d’Erlangen-Nuremberg, Allemagne, a constaté qu’une atteinte articulaire structurale sévère au départ et qu’un nombre initial élevé d’articulations gonflées annonçaient une meilleure réponse à l’abatacept. Les scores Sharp/van der Heijde totaux étaient plus élevés en présence de réponses ACR50 (84,0) et ACR70 (75,8) que d’une réponse ACR20 (36,6). Les réponses ACR50 et ACR70 étaient associées à un nombre moyen de 8,5 et 8,0 articulations gonflées, respectivement, comparativement à 7,0 pour la réponse ACR20. «Il semble donc que les patients atteints d’AP qui présentent des signes d’activité d’ostéoclastes résultant d’une synovite et dont la maladie est évolutive (articulations gonflées et atteinte structurale) seraient de bons candidats pour un traitement par l’abatacept», concluent les chercheurs.
Obtention d’une rémission
Comme à 16 semaines, les résultats à 2 ans de FUTURE 2 – étude de phase III multicentrique de 5 ans à double insu avec placebo et randomisation – ont montré que les patients sous sécukinumab étaient plus nombreux que les patients sous placebo à bénéficier d’une rémission ou d’une faible activité de l’AP. À 2 ans, 29 % et 17 % des patients recevant respectivement 300 mg et 150 mg de sécukinumab étaient en rémission selon l’indice DAPSA (Disease Activity Index for Psoriatic Arthritis), comparativement à 14 % et 10 % à 16 semaines, souligne la Dre Laura Coates, chargée d’enseignement clinique en rhumatologie, University of Oxford, Leeds, Grande-Bretagne. Dans le groupe placebo, seulement 5 % des patients étaient en rémission à 16 semaines (les patients sous placebo passaient au sécukinumab après une nouvelle randomisation à 16 ou à 24 semaines).
Selon une analyse rétrospective de comparaisons sur l’efficacité du sécukinumab (150 mg) et du golimumab (50 mg) chez des patients atteints de SA n’ayant jamais reçu d’agent biologique, la réponse à 24 semaines au sécukinumab était meilleure dans les comparaisons sans prise en compte de l’effet placebo, rapporte le Dr Walter Maksymowych, professeur titulaire de médecine, University of Alberta, Edmonton, Canada.
Ces patients avaient participé à MEASURE 1 et à MEASURE 2 (sécukinumab) ou à GO-RAISE (golimumab). Les données individuelles des deux groupes sécukinumab à 150 mg (n=197) ont été pondérées de façon à coïncider avec les caractéristiques initiales des 138 patients sous golimumab de GO-RAISE. Les groupes placebo de MEASURE 1 et de MEASURE 2 ont aussi été appariés au groupe placebo de GO-RAISE.
Les comparaisons avec prise en compte de l’effet placebo n’ont révélé aucune différence entre le sécukinumab et le golimumab à 12/14 semaines et à 14/16 semaines quant aux taux de réponse partielle ASAS20, ASAS40, et ASAS. À 24 semaines, sans prise en compte de l’effet placebo, les taux de réponse ASAS20 et ASAS40 étaient plus élevéssoussécukinumab, mais les différences par rapport au golimumab n’étaient passignificatives (OR ASAS20 : 1,58; p=0,089 et OR ASAS40 : 1,58; p=0,084).
Questions et réponses
Voici les réponses du Dr Walter Maksymowych, professeur titulaire de médecine, University of Alberta, Edmonton, Canada, à nos questions.
Q : Que pensez-vous des données à 4 ans de MEASURE 1 sur la progression radiographique chez des patients atteints
de SA?
R : Ce suivi montre que la faible progression radiographique est durable sous sécukinumab et qu’elle a été plus lente avec la dose mensuelle de 150 mg qu’avec celle de 75 mg. Le plan novateur de l’étude est intéressant pour l’évaluation de la progression radiographique dans cette maladie. Il faut toutefois préciser que la valeur de p n’est pas fournie; il n’est donc pas clair si la différence entre les deux doses est significative. En outre, les auteurs n’ont pas analysé les éventuelles différences quant aux caractéristiques initiales qui pourraient influer sur la progression radiographique (p. ex. le score mSASSS initial). Les résultats doivent être considérés comme préliminaires d’ici à ce que nous ayons ces données clés.
Q : Pourquoi l’inhibition de la progression radiographique de la maladie importe-t-elle aux patients? A-t-elle des retombées sur l’invalidité? Est-ce un argument en faveur d’une intervention plus précoce?
R : La prévention de la progression radiographique importe aux patients parce que leurs recherches sur Internet leur font voir des cyphoses sévères – qu’ils veulent éviter évidemment. L’ankylose rachidienne a d’importantes répercussions sur l’invalidité, et nous devons continuer de chercher à la prévenir grâce au traitement. Le traitement doit continuer de reposer sur la sévérité des symptômes, mais les cliniciens doivent surtout envisager de prescrire des traitements anti-inflammatoires plus tôt, lorsque des facteurs pronostiques associés à une progression radiographique se présentent.
Q : Chez quels patients atteints d’AP utiliseriez-vous l’échographie ou l’IRM pour mesurer l’atteinte structurale ou sa progression?
R : Nous n’avons pas encore de méthodes validées qui nous permettent