Comptes rendus
Infections fongiques invasives chez les patients sévèrement immunodéprimés : stratégies d’amélioration de la survie globale
Le présent compte rendu est fondé sur des données médicales présentées lors d'un congrès de médecine reconnu ou publiées dans une revue avec comité de lecture ou dans un commentaire signé par un professionnel de la santé reconnu. La matière abordée dans ce compte rendu s'adresse uniquement aux professionnels de la santé reconnus du Canada.
PRESSE PRIORITAIRE - Conférence annuelle 2012 de l’AMMI Canada et de la CACMID
Vancouver, Colombie-Britannique / 3-5 mai 2012
Vancouver - Les infections fongiques invasives (IFI) frappent surtout les patients aux prises avec une h?mopathie maligne qui re?oivent une greffe de cellules souches h?matopo??tiques. Dans la majorit? des cas, il s’agit d’une aspergillose invasive (AI), et le dosage du galactomannane ou du 1,3-b?ta-D-glucane permettrait une d?tection pr?coce. Le traitement pr?emptif de l’AI – c’est-?-dire un traitement pr?coce guid? par des ?l?ments de diagnostic – permet au m?decin d’intervenir lorsque l’infection est encore localis?e et que les chances de survie sont maximales. Jusqu’? tout r?cemment, les associations d’antifongiques ne s’?taient pas r?v?l?es nettement sup?rieures aux antifongiques seuls dans le traitement des AI prouv?es ou probables. Or, pour la premi?re fois, une ?tude men?e ? double insu avec randomisation dont l’objectif ?tait de comparer une bith?rapie et une monoth?rapie dans le traitement d’une AI prouv?e ou probable vient d’objectiver une tendance ? la hausse de la survie, quoique l’?cart n’ait pas ?t? statistiquement significatif. Ces r?sultats donnent ? penser qu’il pourrait y avoir des strat?gies plus efficaces pour le traitement de cette infection grave chez les patients s?v?rement immunod?prim?s.
Rédactrice médicale en chef : Dre Léna Coïc, Montréal, Québec
Fréquentes chez les patients immunodéprimés, les infections fongiques invasives (IFI) sont surtout causées par des espèces aspergillaires. «Il n’est donc pas étonnant que les deux populations les plus à risque d’infection invasive à moisissure soient les greffés et les patients en proie à une hémopathie maligne», affirme le Dr Michel Laverdière, Université de Montréal, Québec. À en juger par des études épidémiologiques, quelque 3,4 % des greffés de cellules souches hématopoïétiques (CSH) développent une IFI au cours d’une année, et il s’agit d’une infection à moisissure dans environ les deux tiers des cas. Les greffés d’organe solide sont à peu près aussi nombreux à développer une IFI avec le temps, mais environ les deux tiers d’entre eux souffrent d’une infection à levure. Les transplantés pulmonaires, pour leur part, sont de loin plus vulnérables aux infections invasives à moisissure qu’aux infections invasives à levure, précise le Dr Laverdière.
Les méthodes dont on dispose actuellement pour diagnostiquer précocement une infection invasive à moisissure sont loin d’être idéales. Les plus exactes pour la détection d’une IFI sont souvent trop risquées chez un patient sévèrement immunodéprimé, et il est difficile de déterminer l’étiologie à l’aide d’examens d’imagerie, indique le Dr Laverdière.
Le dosage du galactomannane (GM) aspergillaire, antigène présent dans la paroi cellulaire de la moisissure, est hautement spécifique de l’aspergillose, mais le dosage du 1,3-bêta-D-glucane peut aussi être très utile même s’il est moins spécifique; de son avis, les deux tests sont dotés d’une capacité prédictive «très comparable», à tout le moins chez les patients neutropéniques. La valeur prédictive du GM dans le liquide de lavage bronchoalvéolaire (LBA) est aussi digne de mention chez les greffés de CSH et les transplantés pulmonaires. «Chez les autres patients, la valeur prédictive du GM dans le liquide de LBA n’est pas aussi bonne», enchaîne le Dr Laverdière.
Diagnostic précoce, traitement critique
On n’insistera jamais assez sur l’importance d’un diagnostic précoce de l’aspergillose invasive (AI) à l’aide d’une méthode diagnostique récente. Les IFI sont associées à un taux de mortalité de presque 97 % lorsque les médecins ont recours aux méthodes diagnostiques traditionnelles, affirme le Pr Ben de Pauw, professeur émérite de médecine, Centre médical universitaire St-Radboud, Nimègue, Pays-Bas. À l’heure actuelle, grâce aux nouvelles techniques telles que le dosage du GM et du 1,3-bêta-D-glucane, on peut abaisser le taux de mortalité jusqu’à 22 %, pour autant que le traitement soit amorcé sans délai. Comme l’explique le Pr de Pauw, les patients étant déjà colonisés, il y a un risque d’AI lorsqu’ils deviennent neutropéniques. En présence de neutropénie fébrile, on leur administre une antibiothérapie, mais ils pourraient en fait souffrir d’une AI et avoir besoin d’un traitement antifongique, même si le diagnostic n’est pas évident.
L’aspergillose est une infection principalement aérogène. Les spores empruntent les voies respiratoires pour pénétrer dans l’organisme et descendent dans les bronches, où apparaissent généralement les premières lésions. À ce stade, l’infection est locale; c’est seulement lorsque le microorganisme envahit d’autres organes que les poumons qu’elle devient invasive. Dans les études où la prophylaxie antifongique était amorcée avant l’apparition du moindre signe d’infection invasive, la prophylaxie n’offrait aucun avantage par rapport au placebo quant à l’incidence de l’AI ou à la mortalité globale, si l’on en juge par une méta-analyse regroupant 38 essais cliniques sur la prophylaxie antifongique (Cancer 2002;94:3230-46).
Le traitement empirique est devenu la norme lorsque la fièvre ne cède pas après 3 ou 4 jours d’antibiothérapie à large spectre, souligne le Pr de Pauw. À vrai dire, «une IFI cliniquement manifeste est très rare en pareilles circonstances», même en l’absence de traitement antifongique empirique, insiste-t-il. Le risque d’apparition d’une IFI est presque nul dans les cas où le profil hémodynamique n’est pas instable, où les examens diagnostiques ne montrent aucun signe d’infection localisée et où le risque n’est pas considéré comme élevé compte tenu de la présence de facteurs de risque connus.
Le Pr de Pauw préconise donc une utilisation beaucoup plus restrictive du traitement empirique des IFI. À son avis, on devrait opter pour un traitement guidé par des éléments de diagnostic, c’est-à-dire sur la foi de la détection d’une infection fongique dans les poumons, et par la présence de facteurs de risque cliniques connus d’IFI, surtout la maladie du greffon contre l’hôte aiguë et toute forme d’anomalie pulmonaire. Une telle approche «préemptive» permettrait aux médecins d’intervenir au début de l’infection et d’offrir aux patients les meilleures chances de survie possible grâce à la mise en route précoce d’un traitement antifongique.
Le Pr de Pauw estime que «si l’on a une vaste expérience de ces infections et que l’on a les installations nécessaires pour reconnaître une IFI débutante, le traitement préemptif est la meilleure façon de faire».
Bithérapie antifongique dans l’AI prouvée ou probable
En sa qualité d’oncologue, le Dr Eric Bow, professeur titulaire de médecine et de microbiologie médicale, University of Manitoba, Winnipeg, voit plusieurs avantages éventuels à l’association d’antifongiques dans le traitement d’une AI prouvée ou probable :
- la possibilité d’une activité accrue grâce à la synergie de deux classes de médicaments;
- un spectre d’activité antifongique plus large;
- la prévention de l’émergence de souches résistantes.
Dans le cadre d’une étude qui a fait date, un traitement de première intention par le voriconazole a donné lieu, chez des patients atteints d’AI, à de meilleurs taux de réponse et à moins d’effets indésirables graves comparativement à l’amphotéricine B, qui était alors le traitement de référence (N Engl J Med 2002;347[6]:408-15). La même étude a également objectivé un gain de survie significatif en faveur de l’antifongique triazolé. À la lumière de cette étude et de notre expérience clinique cumulée, le voriconazole est maintenant recommandé pour le traitement de première intention de l’AI chez la plupart des patients (niveau de preuve : A-I) (IDSA Guidelines for Aspergillosis; CID 2008:46).
Jusqu’à tout récemment, les études qui visaient à explorer l’éventualité de la plus grande efficacité d’une bithérapie antifongique comparativement à la monothérapie dans le traitement d’une AI prouvée ou probable n’avaient pas donné de résultats probants, souligne le Dr Bow. Des chercheurs ont donc entrepris pour la première fois un essai prospectif à double insu avec randomisation afin de comparer une bithérapie et une monothérapie dans le traitement d’une AI prouvée ou probable au sein d’une cohorte de greffés de CSH. Dans cet essai – dont les résultats ont été divulgués au Congrès européen de microbiologie clinique et d’infectiologie (ECCMID) de 2012 (affiche LB 2812) –, les sujets ont été randomisés de façon à recevoir du voriconazole avec ou sans anidulafungine, une échinocandine. La bithérapie a été administrée pendant 2 à 4 semaines, après quoi les patients pouvaient passer à l’antifongique triazolé seul, la durée totale du traitement antifongique ne devant pas excéder 6 semaines. «Le paramètre principal de l’étude était la mortalité toutes causes confondues à 6 semaines», précise le Dr Bow. Au total, 142 patients porteurs d’une AI prouvée ou probable ont été randomisés de façon à recevoir du voriconazole seul et 135 patients, la bithérapie.
Figure 1. Issue des AI probables sur la foi du seul dosage du GM (analyse en intention de traiter modifiée)
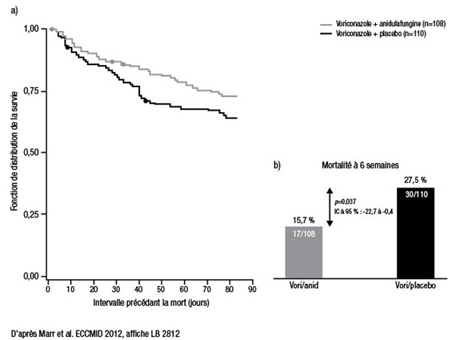
Les chercheurs ont conclu à une AI probable chez 98 % des sujets de la cohorte, et 80 % des diagnostics ont été établis à l’aide d’un résultat positif au dosage du GM, ajoute-t-il. À 6 semaines, le taux de mortalité était plus faible sous bithérapie (19 %) que sous monothérapie (28 %), mais l’écart n’était pas significatif (p<0,09) selon l’analyse en intention de traiter. Cela représente une diminution du risque relatif d’environ 30 % et un nombre de sujets à traiter de 12 pour prévenir 1 décès.
De même, sur le plan de la mortalité toutes causes confondues parmi les patients dont l’AI avait été confirmée par le dosage du GM, l’écart entre le groupe voriconazole + anidulafungine (15,7 %) et le groupe voriconazole seul (27,5 %) était statistiquement significatif à 6 semaines (p=0,037) (Figure 1). «Cet écart représente une diminution du risque relatif de décès de 42 % et un nombre de sujets à traiter de 7, affirme le Dr Bow. Sur le plan de l’innocuité, on n’a observé aucune différence digne de mention entre les patients sous bithérapie et les patients sous monothérapie. C’est le premier essai comparatif avec randomisation à objectiver l’effet [d’une stratégie d’association] sur la survie. Le risque absolu de mortalité a diminué d’environ 12 % et le risque relatif approché de mortalité, d’environ 50 %, Ce sont des résultats bien différents de ce que nous avons observé dans beaucoup d’autres essais», conclut le Dr Bow.