Comptes rendus
Maîtrise actuelle de l’asthme et risque futur d’exacerbation : Stratégies de traitement d’entretien et de secours revisitées
Le présent compte rendu est fondé sur des données médicales présentées lors d'un congrès de médecine reconnu ou publiées dans une revue avec comité de lecture ou dans un commentaire signé par un professionnel de la santé reconnu. La matière abordée dans ce compte rendu s'adresse uniquement aux professionnels de la santé reconnus du Canada.
PERSPECTIVE PROFESSIONNELLE - Point de vue sur l’article suivant : J Allergy Clin Immunol 2010;125(3):600-8.
Mai 2012
Rédacteur en chef invité :
Malcolm Sears, MB, ChB, FRACP, FRCPC, FAAAAI
Professeur titulaire de médecine
Division de pneumologie
St. Joseph’s Healthcare
Titulaire d’une chaire d’épidémiologie
en pneumologie
financée par un fonds de dotation
McMaster University
Hamilton (Ontario)
Introduction
Dans le diabète et l’hypertension, il est notoire que la diminution du risque de complications passe respectivement par l’équilibre glycémique et l’atteinte de la tension artérielle cible. Dans l’asthme, en revanche, le concept est récent. L’étude GOAL (Gaining Optimal Asthma ControL) a été la première à montrer que la maîtrise de l’asthme – telle que définie par les guides de pratique – était avantageuse à long terme et, en particulier, qu’elle diminuait le nombre d’exacerbations aiguës. Cela dit, de nombreux sujets de l’étude GOAL présentaient un asthme léger (volume expiratoire maximal en 1 seconde [VEMS] moyen de 75 % ou plus) à leur admission à l’étude; de plus, environ le tiers d’entre eux n’avaient jamais reçu de corticostéroïdes en inhalation (CSI). Afin de déterminer si la maîtrise de l’asthme dans le moment présent influe sur le risque futur en présence d’un asthme plus sévère, des chercheurs ont colligé les résultats de cinq études distinctes sur l’utilisation d’un seul et même inhalateur combinant un CSI et un bronchodilatateur à longue durée d’action (BALA) et à début d’action rapide pour le traitement d’entretien et le traitement de secours de l’asthme. Les résultats ont été comparés à ceux d’autres traitements d’entretien et de secours chez des patients atteints d’asthme modéré à sévère. Cette analyse a révélé que si le traitement d’entretien combiné au traitement de secours permettait d’obtenir un niveau similaire de maîtrise de l’asthme, il réduisait néanmoins le risque futur d’instabilité et d’exacerbations plus efficacement. Il a été démontré que les patients dont les exacerbations étaient fréquentes, comparativement aux patients dont les exacerbations étaient moins fréquentes, présentaient un déclin annuel significativement plus marqué de la fonction pulmonaire. Par conséquent, une fréquence moindre d’exacerbations pourrait contribuer à réduire le déclin progressif de la fonction pulmonaire, facteur important à considérer en présence d’asthme sévère.
L’étude GOAL
Sous la direction de l’auteur principal, Eric Bateman1, University of Cape Town, Afrique du Sud, les investigateurs de l’étude GOAL (Gaining Optimal Asthma ControL) ont tenté de déterminer s’il était possible de maîtriser l’asthme selon les critères définis par les guides de pratique. Ainsi, quelque 3421 patients atteints d’asthme non maîtrisé ont été randomisés de façon à recevoir l’un ou l’autre des traitements de fond suivants : fluticasone ou salmétérol/fluticasone. Au cours de la phase I, la dose était ajustée à la hausse jusqu’à ce que l’asthme soit totalement maîtrisé ou que la dose maximale de 500 µg de corticostéroïdes, 2 fois/jour, soit atteinte. Au cours de la phase II, les patients continuaient de recevoir une dose stable jusqu’à la fin de l’étude d’une durée de 1 an. Même si les patients n’avaient jamais été exposés à des corticostéroïdes ou s’ils avaient au contraire déjà pris des doses faibles ou modérées de corticostéroïdes lorsqu’ils ont été admis à l’étude, l’asthme a pu être totalement maîtrisé chez un certain pourcentage de patients de chaque sous-groupe. Les patients de chaque sous-groupe recevant l’association étaient significativement plus nombreux à parvenir à une maîtrise totale ou à une bonne maîtrise que les patients recevant uniquement le corticostéroïde en inhalation (CSI). Dans la majorité des cas, lorsque l’asthme était maîtrisé au terme de la phase I (ajustement posologique), il était aussi maîtrisé au terme de la phase II (dose stable).
L’étude GOAL a été la première à montrer que la maîtrise – telle que définie par les guides de pratique – pouvait être atteinte et maintenue chez la majorité des patients souffrant d’asthme de sévérité variable et que la maîtrise de l’asthme s’accompagnait d’un très faible taux d’exacerbations. Même lorsque la maîtrise de l’asthme ne répondait pas strictement à tous les critères prévus au protocole, les chercheurs ont observé une diminution du taux d’exacerbations et une amélioration de l’état de santé au cours des 12 mois de l’étude.
Lorsqu’ils ont de nouveau analysé les données de l’étude GOAL quelques années plus tard2, Bateman et ses collaborateurs se sont penchés sur le lien entre le niveau de maîtrise de l’asthme atteint durant la phase I (ajustement posologique) et la stabilité de cette maîtrise durant la phase d’entretien (phase II). Là encore, dans les trois sous-groupes de patients exposés ou non exposés aux corticostéroïdes, les patients dont l’asthme était totalement maîtrisé au terme de la phase I ont bénéficié d’une maîtrise totale pendant le plus clair de la phase II; une fois que la maîtrise totale avait été atteinte au cours de la phase I, elle se maintenait pendant au moins 3 mois. Les données indiquent également qu’une maîtrise plus serrée de l’asthme au terme de la phase I était prédictive d’une probabilité plus forte de maîtrise au cours de la phase II.
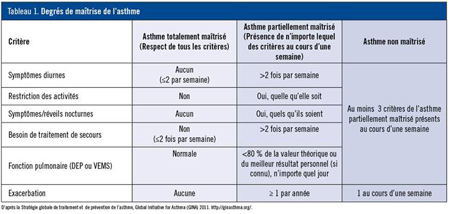
Tableau 1.
En effet, la probabilité de maîtrise totale au cours de la phase II était 30 fois supérieure dans le groupe de patients dont l’asthme était totalement maîtrisé au terme de la phase I comparativement à ceux du groupe dont l’asthme était maîtrisé de façon insatisfaisante (OR 30,5, p<0,001) et près de 7 fois supérieure comparativement à ceux du groupe dont l’asthme était maîtrisé de façon satisfaisante au terme de la phase I (OR 6,63, p<0,001).
Les résultats de cette analyse post-hoc montrent une fois de plus qu’une maîtrise durable de l’asthme pendant 8 semaines diminue grandement le risque d’instabilité, que l’on mesure en calculant le nombre de semaines où l’asthme n’est pas bien maîtrisé. Inversement, les sujets de GOAL dont l’asthme était maîtrisé de façon insatisfaisante ou satisfaisante étaient plus susceptibles de consulter un médecin en dehors des visites prévues. La stabilité de la maîtrise est donc essentielle à la réduction du risque d’exacerbation, et le patient a plus de chances de parvenir à la stabilité lorsqu’il adhère à son traitement sans faille.
Piètre maîtrise de l’asthme
Une piètre maîtrise de l’asthme est associée à un risque accru d’exacerbation, d’hospitalisation et de visite aux urgences. En outre, il a été démontré qu’une maîtrise instable nuisait considérablement à la qualité de vie et qu’elle avait des conséquences à la fois psychosociales et économiques. De même, à la suite d’un processus que l’on qualifie souvent de «remodelage», on observe une perte accélérée de la fonction pulmonaire chez les patients dont l’asthme est mal maîtrisé. Dans une autre étude, Bai et al.3 ont évalué l’effet d’exacerbations sévères – que le protocole définissait soit par une hospitalisation pour aggravation de l’asthme, soit par une baisse significative et réversible du volume expiratoire maximal en 1 seconde (VEMS) – sur la progression de l’obstruction des voies respiratoires chez 93 non-fumeurs atteints d’asthme modéré à sévère. La durée médiane du suivi était de 11 ans. Comparativement aux patients dont les exacerbations étaient moins fréquentes, les patients dont les exacerbations étaient fréquentes présentaient un déclin annuel significativement plus marqué du VEMS et une aggravation de l’obstruction des voies respiratoires après 11 ans de suivi. Chez les patients dont le nombre d’exacerbations était supérieur au nombre médian d’exacerbations ou chez ceux dont le nombre d’exacerbations était inférieur à la médiane, les chercheurs ont noté un déclin du VEMS de 31,5 mL·année-1 et de 6,5 mL·année-1, respectivement. Dans la même étude, chaque exacerbation sévère était prédictive d’un déclin supplémentaire de 30 mL·année-1.
Résultats d’une analyse rétrospective
L’évaluation de l’hypothèse voulant qu’un traitement efficace puisse prévenir le déclin de la fonction pulmonaire a donné des résultats ambigus, mais il serait logique que la diminution du nombre d’exacerbations contribue à préserver la fonction pulmonaire. À l’aide d’une base de données regroupant cinq études où l’association budésonide/formotérol en traitement d’entretien et de secours avait été comparée à trois autres schémas d’entretien, Bateman4 et son équipe multicentrique ont étudié le lien entre la maîtrise telle que définie par le résultat initial au questionnaire ACQ-5 (Asthma Control Questionnaire) et/ou la maîtrise clinique telle que définie par GINA (Global Initiative for Asthma) (Tableau 1), d’une part, et le risque futur d’instabilité et d’exacerbations, d’autre part.
Dans cette base de données, les schémas de comparaison étaient : CSI à dose plus forte; CSI à la même dose/bêta-agoniste à longue durée d’action (BALA); et CSI à dose plus forte/BALA. Un bêta-agoniste à courte durée d’action (BACA) était utilisé en traitement de secours avec les trois schémas de comparaison. D’une durée de 6 ou 12 mois, chacune des études incluses dans l’analyse rétrospective avait comme paramètre principal le délai d’apparition de la première exacerbation sévère. Pour les besoins de l’analyse, on entendait par «exacerbation sévère» la détérioration de la maîtrise de l’asthme ayant pour conséquence l’hospitalisation du patient, un traitement au service des urgences et/ou l’utilisation de corticostéroïdes oraux.
La maîtrise globale de l’asthme selon GINA était définie par plusieurs critères et, dans le cadre de trois études, les patients s’autoévaluaient lors des visites à la clinique à l’aide du questionnaire ACQ-5. Le VEMS initial moyen était d’environ 72 % dans tous les groupes de traitement; la dose moyenne de CSI s’élevait à environ 700 µg/jour, et entre le tiers et la moitié des patients recevaient aussi un traitement par BALA. Le pourcentage moyen de jours sans symptômes variait entre environ 10 et 17 %, et l’ancienneté médiane de l’asthme était d’environ 11 ans.
Les analyses ont révélé que le pourcentage de patients parvenant à une maîtrise totale ou totale/partielle pendant une semaine selon les critères de GINA augmentait graduellement durant les études, quel qu’ait été le traitement utilisé, mais l’amélioration s’observait en majeure partie au cours des 3 à 6 premiers mois de traitement. Au sein de chaque étude, le pourcentage de patients dont l’asthme était maîtrisé totalement ou partiellement était similaire pour l’association budésonide/formotérol en traitement d’entretien et de secours et les trois autres schémas de comparaison : 56 % vs 45 % pour le schéma CSI à dose plus forte; 56 % vs 53 % pour le schéma CSI à la même dose/BALA; et 54 % vs 54 % pour le schéma CSI à dose plus forte/BALA.
Les auteurs ont aussi constaté que plus la maîtrise de l’asthme était serrée, plus la probabilité de maintien de cette maîtrise était élevée et plus le risque d’exacerbation au cours des semaines subséquentes était faible. Il importe surtout de souligner que, chaque semaine, les patients du groupe budésonide/formotérol en traitement d’entretien et de secours étaient moins nombreux que les sujets des trois autres groupes à avoir besoin de soins médicaux (Figure 1).
Figure 1. Patients ayant eu besoin de soins médicaux pour une exacerbation
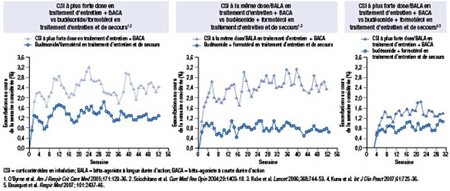
Fait peut-être tout aussi important, il y a eu moins d’hospitalisations dans le groupe budésonide/salmétérol que dans le groupe salmétérol à la dose maximale/fluticasone (9 vs 13 pour 100 patients/année; p=0,046) ainsi que moins d’exacerbations (25 vs 31 pour 100 patients/année, respectivement; p=0,039). La dose moyenne de CSI était aussi significativement plus faible dans le groupe budésonide/formotérol en traitement d’entretien et de secours : 1238 µg/jour vs 2000 µg/jour dans le groupe CSI à la dose maximale (p<0,0001).
Discussion
Si l’on y regarde de plus près, les résultats de cette analyse groupée font ressortir quelques points. Il importe d’abord de reconnaître que pour des patients souffrant d’un asthme de sévérité comparable à ce qu’on a observé dans l’étude, la maîtrise totale est un objectif très difficile à atteindre, tant en recherche clinique que dans la pratique clinique, et il est certes digne de mention que les quatre schémas aient été associés à des taux comparables de maîtrise. C’est donc dire que, sous réserve d’une utilisation conforme aux directives du médecin, la plupart des schémas antiasthmatiques sont efficaces. Cela dit, même si les quatre schémas ont autorisé des taux comparables de maîtrise, le pourcentage plus faible de patients ayant eu des exacerbations dans le groupe budésonide/formotérol en traitement d’entretien et de secours donne tout lieu de croire que le corticostéroïde offre un avantage supplémentaire lorsque se dessine une exacerbation et que ce «coup de pouce» anti-inflammatoire supplémentaire pourrait faire échec à l’exacerbation imminente chez certains patients. En revanche, comme le traitement de secours utilisé avec les trois autres schémas de comparaison se résumait à un BACA en monothérapie, les patients ne bénéficiaient que d’un effet bronchodilatateur supplémentaire lors d’une exacerbation et non d’un «coup de pouce» anti-inflammatoire supplémentaire.
L’association CSI à forte dose/BALA s’est révélée plus efficace que l’association CSI à faible dose/BALA, mais cette dernière a tout de même été plus efficace que le CSI à forte dose en monothérapie. L’amélioration que l’on a observée chez tous les patients avec le temps reflète aussi ce que nous savons au sujet d’une bonne maîtrise de l’asthme. Lorsqu’un patient participe à une étude, on lui explique quoi faire et, en général, son adhésion au traitement est meilleure du fait que le suivi est étroit et qu’on l’encourage à persévérer. Autrement dit, la plupart des patients se portent mieux s’ils prennent leur traitement tel qu’il leur a été prescrit. C’est vrai également dans la pratique clinique : si le patient adhère à son traitement, il peut s’attendre à aller mieux à court et à plus long terme.
Du point de vue de l’observance du traitement, le plus important est probablement de convaincre les patients, du moins ceux qui souffrent d’asthme modéré à sévère, de ne pas mettre fin à leur traitement lorsqu’ils commencent à se sentir mieux et de ne pas utiliser leur inhalateur uniquement quand ils pensent en avoir besoin. De même, on doit aider les parents à différencier les effets indésirables réels des effets indésirables qu’ils redoutent concernant l’utilisation prolongée des CSI à faible dose chez les enfants et on doit leur faire comprendre que les enfants atteints d’asthme modéré à sévère doivent prendre régulièrement leur traitement. Face à un nouveau patient, nous devrions toujours demander à un éducateur spécialisé de montrer la bonne technique d’inhalation au patient ou à ses parents et nous assurer qu’ils y parviennent. Le médecin doit aussi garder à l’esprit que l’observance est essentielle à la maîtrise actuelle et future de l’asthme et qu’il doit encourager ses patients à demeurer observants lors de chaque visite.
Résumé
Des études antérieures et les analyses groupées rapportées par Bateman et al. montrent clairement que le risque d’exacerbation et de déclin de la fonction pulmonaire diminue lorsque le patient parvient à une bonne maîtrise de l’asthme et qu’il la maintient. Les données étayent l’utilisation combinée d’un CSI et d’un bronchodilatateur à longue durée d’action et à début d’action rapide à la fois pour le traitement de fond et le traitement symptomatique de l’asthme et, surtout, elles montrent que ce schéma se distingue principalement des autres du fait qu’il est associé à un nombre moindre d’exacerbations. Cela dit, si efficace que soit un schéma en inhalation particulier, son efficacité sera optimale uniquement si le patient a été éduqué et s’il suit son traitement tel qu’il lui a été prescrit. Le médecin a donc un rôle clé à jouer : il doit aider le patient à comprendre les avantages de l’adhésion au traitement, notamment une maîtrise durable de l’asthme qui se traduira par une protection accrue contre les exacerbations futures et contre le déclin progressif de la fonction pulmonaire.
Référence
1. Bateman et al. Am J Respir Crit Care Med 2004;170:836-44.
2. Bateman et al. Allergy 2008;63:932-38.
3. Bai et al. Eur Respir J 2007;30:452-56.
4. Bateman et al. J Allergy Clin Immunol 2010;125:600-8.