Comptes rendus
Institut de cardiologie de l’Université d’Ottawa
Le présent compte rendu est fondé sur des données médicales présentées lors d'un congrès de médecine reconnu ou publiées dans une revue avec comité de lecture ou dans un commentaire signé par un professionnel de la santé reconnu. La matière abordée dans ce compte rendu s'adresse uniquement aux professionnels de la santé reconnus du Canada.
PERSPECTIVE PROFESSIONNELLE - L’heure est au PROTOCOLE - Point de vue régional sur les preuves et les changements qui en découlent
mai 2013
Sous la direction de :
Michel Le May, MD, FRCPC
Directeur, Unité de soins coronariens et Programme régional STEMI de l’Institut de cardiologie de l’Université d’Ottawa
Professeur titulaire de médecine
Institut de cardiologie de l’Université d’Ottawa
Ottawa (Ontario)
Introduction
L’Institut de cardiologie de l’Université d’Ottawa (ICUO) a récemment modifié son protocole de traitement antiplaquettaire dans la prise en charge des syndromes coronariens aigus (SCA). La nouvelle stratégie – dont l’objectif est de réduire significativement le risque d’événement cardiovasculaire (CV) majeur – consiste principalement à remplacer l’antiplaquettaire de référence antérieur, le clopidogrel, par l’un des nouveaux antiplaquettaires. Étayés par les résultats des essais cliniques d’envergure qui ont motivé la mise à jour de l’algorithme, les traitements recommandés ouvrent la porte à des gains cliniques découlant d’un effet antiplaquettaire plus marqué, y compris, dans certains cas, un risque moindre de décès. Ces avantages s’accompagnent d’un risque faible et acceptable d’hémorragie majeure ou mineure. Comme il est fondamentalement important de désactiver les plaquettes pour modifier l’évolution naturelle d’un SCA, on doit forcément optimiser le traitement antiplaquettaire si l’on aspire à améliorer le pronostic des SCA. Précisons enfin que le nouveau protocole est compatible avec la mise à jour des recommandations nationales.
Traitement de référence antérieur : une amélioration s’imposait
Pendant plus de 10 ans, la bithérapie antiplaquettaire clopidogrel + AAS a été la norme dans la prise en charge des SCA, mais le taux d’événements CV chez les victimes d’un SCA demeurait assez élevé. Lors de l’essai phare CURE, on a signalé un infarctus du myocarde (IM) récidivant, un AVC ou un décès d’origine CV chez 9,3 % des sujets sous clopidogrel + AAS malgré une diminution de 20 % par rapport à l’AAS seul1. Cette étude a été réalisée chez des patients ayant subi un IM sans sus-décalage du segment ST (NSTEMI). Lors de l’essai CLARITY-TIMI 28, qui ciblait plutôt des patients ayant subi un IM avec sus-décalage du segment ST (STEMI), le risque résiduel de décès, d’IM récidivant ou d’ischémie récurrente nécessitant une intervention de revascularisation urgente s’élevait à 11,6 % dans le groupe clopidogrel + AAS malgré une diminution de 20 % du risque par rapport au groupe placebo2.
Depuis le jour où ces études ont fait de la bithérapie clopidogrel + AAS le traitement de référence des SCA, deux essais d’envergure sur les SCA ont prouvé qu’un traitement antiplaquettaire plus efficace pouvait réduire davantage le risque CV. Dans l’un de ces essais, le ticagrelor était administré à tous les patients en proie à un SCA qui se présentaient à l’hôpital3. Dans l’autre, le prasugrel était administré à des patients en proie à un SCA qui étaient censés subir une intervention coronarienne percutanée (ICP)4. Les données de ces essais nous permettent d’envisager de meilleurs résultats qu’avec le traitement de référence antérieur clopidogrel + AAS.
Dans le cadre de l’essai TRITON TIMI-38, 13 608 patients en proie à un SCA qui devaient subir une ICP ont été randomisés. Les patients du groupe expérimental recevaient une dose d’attaque de prasugrel (60 mg) suivie d’une dose d’entretien de prasugrel (10 mg/jour), alors que le groupe de comparaison recevait une dose d’attaque de clopidogrel (300 mg) suivie d’une dose d’entretien de clopidogrel (75 mg/jour). Les deux groupes recevaient de l’AAS. Environ 25 % des SCA étaient des STEMI; les autres étaient des NSTEMI.
Par comparaison au clopidogrel, le prasugrel a diminué le risque relatif de survenue d’un événement compris dans le paramètre mixte (mort imputable à un événement CV, IM ou AVC) de 19 % (HR 0,81; p<0,001) et le risque absolu, de 2,2 % (9,9 % des sujets sous prasugrel vs 12,1 % des témoins). Le risque relatif d’hémorragie majeure a augmenté de 32 % sous prasugrel (HR 1,32; p=0,03) et le risque absolu, de 0,6 % (hémorragie majeure chez 2,4 % des patients sous prasugrel vs 1,8 % des témoins). Il n’y avait toutefois aucune différence sur le plan de la mortalité. Les auteurs ont conclu qu’il fallait soupeser la protection accrue contre les récidives ischémiques en regard du risque hémorragique accru. Des analyses post hoc ont toutefois permis d’orienter la sélection des candidats.
Dans l’essai PLATO, tous les sujets admis à l’hôpital pour un SCA ont été randomisés sans égard à l’intervention qu’ils allaient subir ou au traitement antiplaquettaire qu’ils avaient reçu avant leur hospitalisation. Le groupe expérimental recevait une dose d’attaque de ticagrelor (180 mg), puis une dose d’entretien de ticagrelor (90 mg 2 fois/jour), tandis que le groupe de comparaison recevait une dose d’attaque de clopidogrel (300 ou 600 mg), puis une dose d’entretien de clopidogrel (75 mg/jour). Les deux groupes recevaient de l’AAS. Environ 37 % des 18 624 patients randomisés avaient eu un STEMI et les autres, un NSTEMI.
Par rapport au clopidogrel, le ticagrelor a diminué le risque relatif de survenue d’un événement compris dans le paramètre mixte (décès d’origine vasculaire, IM ou AVC) de 16 % (HR 0,84; p<0,001) et le risque absolu, de 1,9 % (9,8 % vs 11,7 % des sujets sous ticagrelor et clopidogrel, respectivement). Sur le plan des hémorragies majeures totales, l’écart entre les deux groupes n’a pas atteint le seuil de significativité statistique (11,6 % sous ticagrelor vs 11,2 %; p=0,43), mais les hémorragies majeures non liées à un pontage aortocoronarien (PAC) étaient significativement plus fréquentes (4,5 % vs 3,8 %; p=0,026). Fait unique dans un essai sur des antiplaquettaires, le ticagrelor a été associé à une diminution de 22 % de la mortalité toutes causes confondues : 5,9 % vs 4,9 % (HR 0,78; valeur nominale de p<0,001).
Mise en application des nouvelles données
La mise à jour des normes de traitement antiplaquettaire chez les patients en proie à un SCA devrait nous permettre d’améliorer les résultats si l’on en juge par les essais PLATO et TRITON-TIMI 38. Si l’administration d’AAS s’impose d’emblée dans tous les SCA, le choix du deuxième antiplaquettaire dépend du diagnostic, de la stratégie d’intervention et des caractéristiques du patient. Plusieurs organismes importants ont actualisé leurs recommandations de traitement antiplaquettaire en cas de SCA à la lumière des résultats des essais PLATO et TRITON-TIMI 38, mais il demeure approprié que les régions et les établissements élaborent leurs propres algorithmes en raison des différences d’une région ou d’un hôpital à l’autre quant à l’organisation des soins pour les SCA.
À l’ICUO, nous avons opté pour le ticagrelor comme substitut standard du clopidogrel dans le cadre d’une double stratégie antiplaquettaire avec AAS pour la plupart des cas de SCA. Toute bithérapie antiplaquettaire commande la prudence chez un patient déjà sous anticoagulant oral. Le cardiologue d’intervention pourra envisager le clopidogrel plutôt que le ticagrelor chez les patients qui reçoivent un anticoagulant oral, y compris la warfarine, et chez les patients ayant des antécédents d’hémorragie intracrânienne.
Chez les patients en proie à un STEMI qui doivent subir une ICP, le prasugrel s’est révélé plus efficace que le clopidogrel en association avec l’AAS dans le cadre d’une bithérapie antiplaquettaire, mais le ratio bénéfice:risque variait dans les divers sous-groupes de la population principale, ce qui a donné lieu à d’importantes exceptions, notamment chez les patients de plus de 75 ans et les patients de poids inférieur à 60 kg. Nous avons tenu compte des résultats des essais TRITON-TIMI 38 et PLATO, mais pour simplifier et rationaliser le processus thérapeutique, l’ICUO a porté son choix sur le ticagrelor dans le traitement des STEMI. Dans les cas où le médecin traitant considère le ticagrelor comme inapproprié, le clopidogrel demeure une option.
Pertinence du nouvel algorithme
dans les centres régionaux
La Société canadienne de cardiologie a publié en 2012 ses recommandations de traitement antiplaquettaire en cas de SCA5. Ces recommandations – qui ont fortement influé sur les choix de l’ICUO – mettent l’accent sur le remplacement du clopidogrel par le ticagrelor, tant pour les STEMI que pour les NSTEMI (classe 1). Le clopidogrel est maintenant relégué au deuxième rang. Le prasugrel est aussi une option chez les victimes d’un STEMI, mais les données à l’appui de son utilisation proviennent de l’essai TRITON-TIMI 38, lors duquel on vérifiait l’anatomie du cœur du patient avant d’amorcer le traitement.
Les nouvelles recommandations en vigueur à l’ICUO reposent sur plusieurs hypothèses qui ne s’appliquent pas forcément aux centres communautaires avoisinants. En particulier, l’utilisation du prasugrel chez la victime d’un STEMI dépend de l’accès à une salle de cathétérisme et de la possibilité de réaliser une ICP. Évidemment, compte tenu des disparités au sein de la région dans la prise en charge d’un SCA, principalement imputables à la variabilité des ressources – notamment la proximité des équipes d’intervention rapide –, on doit adapter les recommandations thérapeutiques aux réalités régionales. Tout en gardant ces contraintes à l’esprit, on doit retenir que les pratiques habituelles dans les grands centres de la région s’appliquent aux hôpitaux communautaires et qu’on ne doit rater aucune occasion d’améliorer les résultats en utilisant des schémas antiplaquettaires plus efficaces.
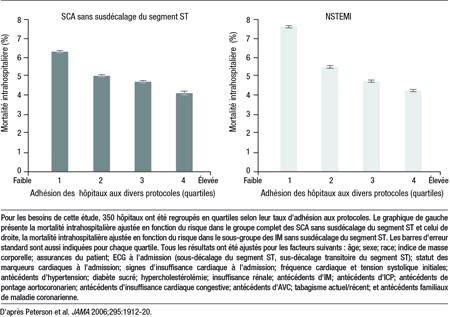
De solides données nous permettent de conclure que le recours à des stratégies plus modernes chez les sujets appropriés améliore les résultats du traitement des SCA et peut même diminuer la mortalité. Dans la prise en charge des SCA, la mise en application de recommandations thérapeutiques a été associée à une amélioration statistiquement significative des résultats. Dans le cadre d’une étude d’observation qui regroupait 350 centres universitaires et non universitaires, à chaque augmentation de 10 % de l’adhésion aux recommandations factuelles correspondait une diminution de 10 % de la mortalité intrahospitalière (Figure 1)6.
Figure 1. Association entre le taux d’adhésion des hôpitaux aux protocoles et la mortalité intrahospitalière
Conclusion
Les stratégies antiplaquettaires de première intention dans la prise en charge des SCA ont été révisées. Le ticagrelor et le prasugrel, deux nouveaux agents, nous donnent une bonne occasion d’améliorer les résultats par rapport au clopidogrel lorsqu’ils sont associés à l’AAS. Chez les victimes d’un SCA, le ticagrelor est devenu l’agent de choix en raison de ses avantages, notamment une diminution nominale de la mortalité. L’ICUO a formulé ses recommandations expressément pour permettre à ses médecins de repérer ces occasions dans le cadre d’une stratégie simplifiée et facile à appliquer.
Questions et réponses
Q : Que pensez-vous du ratio bénéfice:risque des nouveaux antiplaquettaires dans le contexte des recommandations que l’on a actualisées pour diminuer le risque de thrombose tout en maintenant un taux acceptable d’hémorragies?
R : Dans l’essai TRITON-TIMI 38, le prasugrel a été associé après 15 mois à un taux moindre de thrombose sur endoprothèse : 1,1 % vs 2,4 % pour le clopidogrel (p<0,001). Par contre, le taux d’hémorragies majeures TIMI non liées à un PAC a atteint 2,4 % sous prasugrel, par comparaison à 1,8 % sous clopidogrel (p=0,03) et le taux d’hémorragies mortelles, 0,4 % vs 0,1 % respectivement (p=0,002). Chez les patients ayant des antécédents d’AVC ou d’ischémie cérébrale transitoire (ICT), le taux d’hémorragies intracrâniennes était plus élevé sous prasugrel (2,3 % vs 0 % pour le clopidogrel, p=0,02). En raison de ces résultats, il n’est pas recommandé de prescrire du prasugrel à un patient ayant des antécédents d’ICT ou d’AVC.
Dans l’essai PLATO, on a aussi observé une diminution significative du nombre de thromboses sur endoprothèse probables ou confirmées sous ticagrelor, comparativement au clopidogrel : 2,2 % vs 2,9 % (p=0,02). Une hémorragie considérée comme majeure selon les critères de l’essai PLATO a été signalée chez 11,6 % des patients sous ticagrelor vs 11,2 % des patients sous clopidogrel (p=0,43). Une hémorragie considérée comme majeure selon les critères TIMI a été rapportée chez 7,9 % et 7,7 % des patients sous ticagrelor et sous clopidogrel, respectivement (p=0,57). Par contre, le taux d’hémorragies majeures TIMI non liées à un PAC était significativement plus élevé sous ticagrelor (2,8 % vs 2,2 % sous clopidogrel; p=0,03). Chez les patients qui avaient des antécédents d’AVC, le ticagrelor n’a pas été associé à un taux plus élevé d’hémorragie intracrânienne; le taux d’hémorragies mortelles se chiffrait à 0,3 % dans chaque groupe.
Q : Les essais qui ont motivé l’actualisation des recommandations comparaient des antiplaquettaires dans différents sous-groupes de patients. Pourquoi, à votre avis, était-il important de prouver la supériorité du prasugrel ou du ticagrelor sur le clopidogrel dans différents types de SCA (STEMI, NSTEMI, angor instable, etc.)?
R : Les STEMI et les NSTEMI ont le même facteur déclenchant, à savoir la rupture d’une plaque, mais les tableaux cliniques diffèrent à certains égards. En général, le STEMI est plus aigu et s’accompagne d’une inflammation plus marquée qui peut nuire significativement à l’absorption et au métabolisme de l’antiplaquettaire. Les propriétés pharmacocinétiques et pharmacodynamiques peuvent aussi être modifiées chez ces patients. Dans le contexte d’une ICP primaire, l’antiplaquettaire doit agir rapidement pour prévenir une thrombose sur endoprothèse. Les deux essais phares, TRITON TIMI-38 et PLATO, ont tous deux montré que, comparativement au clopidogrel, les nouveaux antiplaquettaires, le prasugrel et le ticagrelor respectivement, étaient associés à un bénéfice significativement plus marqué, tant en cas de STEMI que de NSTEMI. Les bénéfices associés aux nouveaux antiplaquettaires s’appliquent donc à la fois aux STEMI et aux NSTEMI.
Q : Que pensez-vous des éventuels effets indésirables des nouveaux antiplaquettaires compte tenu des meilleurs résultats qu’ils permettent d’obtenir?
R : La bithérapie antiplaquettaire reposant sur l’association du ticagrelor ou du prasugrel et de l’AAS risque davantage que l’AAS seul d’entraîner des complications hémorragiques. Les saignements incommodants comme une tendance à faire des ecchymoses sont assurément plus fréquents.
L’essai TRITON-TIMI 38 a révélé que le prasugrel était associé à un risque hémorragique accru comparativement au clopidogrel. De plus, les patients ayant des antécédents d’AVC ou d’ICT étaient plus à risque d’hémorragie intracrânienne. Le prasugrel est donc contre-indiqué en présence d’antécédents d’AVC ou d’ICT. En outre, le prasugrel a été associé à une augmentation des hémorragies chez les patients recevant un PAC. Il faut donc soupeser l’utilité du prasugrel à la fois en fonction des complications hémorragiques et de l’efficacité du traitement sur les plans de la mortalité, des IM récidivants ou des AVC, et des thromboses sur endoprothèse.
Dans l’essai PLATO, le ticagrelor n’a pas été associé à un risque accru d’hémorragie. Par contre, chez les patients qui n’ont pas eu besoin d’un PAC, le ticagrelor a été associé à un taux plus élevé d’hémorragies. Une dyspnée a été signalée chez 13,8 % des patients sous ticagrelor, par comparaison à 7,8 % des patients sous clopidogrel. La dyspnée, croit-on, serait associée à un mécanisme faisant intervenir l’adénosine. Ce symptôme – qui n’était pas lié à une anomalie de la fonction pulmonaire – est généralement d’intensité légère et disparaît de lui-même. Chez quelques patients, la dyspnée peut être sévère et il faut alors remplacer le ticagrelor par le clopidogrel. Fait digne de mention, le traitement a dû être arrêté chez seulement 0,9 % des sujets de PLATO sous ticagrelor. Il faut bien sûr soupeser les effets indésirables du ticagrelor en regard de ses bénéfices, à savoir une diminution des événements ischémiques, y compris une diminution des thromboses sur endoprothèse et, surtout, de la mortalité.
Q : La nouvelle stratégie comporte des points de décision qui n’y étaient pas lorsque tous les patients recevaient du clopidogrel et de l’AAS. Que doit-on faire pour améliorer les résultats?
R : Les nouveaux agents ont été étudiés dans le contexte d’un SCA. Selon les nouvelles recommandations en vigueur au Canada, le ticagrelor ou le prasugrel devrait remplacer le clopidogrel dans la prise en charge des SCA, et le traitement devrait durer 1 an. Le patient sous fibrinolytique fait toutefois exception à la règle. S’il a moins de 75 ans, le traitement de référence se résume toujours à une dose d’attaque de clopidogrel de 300 mg au moment de l’administration du fibrinolytique suivie d’une dose d’entretien de clopidogrel de 75 mg/jour. S’il a 75 ans ou plus, on recommande d’amorcer le traitement avec 75 mg/jour de clopidogrel seulement, c’est-à-dire sans dose d’attaque. À l’heure actuelle, aucune donnée n’étaye l’utilité des nouveaux agents en présence d’angine stable. Dans les cas où l’ICP n’est pas urgente, le traitement devrait reposer sur l’association clopidogrel + AAS. En outre, nous ne disposons d’aucune donnée sur le traitement au long cours par une bithérapie antiplaquettaire reposant sur les nouveaux agents. L’essai PEGASUS – en cours – évalue l’association ticagrelor + AAS chez les patients stables ayant des antécédents d’IM. Le recrutement de cet essai vient tout juste de se terminer.
Références
1. Yusuf et al. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST-segment elevation. N Engl J Med 2001;345(7):494-502.
2. Sabatine et al. Addition of clopidogrel to aspirin and fibrinolytic therapy for myocardial infarction with STsegment elevation. N Engl J Med 2005;352(12):1179-89.
3. Wallentin et al. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009;361(11):1045-57.
4. Wiviott et al. Prasugrel versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2007;357(20):2001-15.
5.http://www.ccsguidelineprograms.ca/images/stories/AP_Therapy/2012/ccs_ap_guidelinesrecomendations_oct2012.pdf.
6. Peterson et al. Association between hospital process performance and outcomes among patients with acute coronary syndromes.
JAMA 2006;295(16):1912-20.