Comptes rendus
Nouveaux antiviraux à action directe dans le traitement de l’infection par le virus de l’hépatite C de génotype 1
Le présent compte rendu est fondé sur des données médicales présentées lors d'un congrès de médecine reconnu ou publiées dans une revue avec comité de lecture ou dans un commentaire signé par un professionnel de la santé reconnu. La matière abordée dans ce compte rendu s'adresse uniquement aux professionnels de la santé reconnus du Canada.
PERSPECTIVE PROFESSIONNELLE - Point de vue sur les communications présentées à la 49e Assemblée annuelle de la European Association for the Study of the Liver (EASL)
Londres, Royaume-Uni / 9-13 avril 2014
Sous la direction de :
Jordan J. Feld, MD, MPH
Toronto Centre for Liver Disease
Toronto Western Hospital
Francis Family Liver Clinic
University Health Network
McLaughlin-Rotman Centre for Global Health
Toronto, Canada
Introduction
L’avènement d’une ère nouvelle dans le traitement de l’infection par le virus de l’hépatite C (VHC) – 25 ans après la découverte du VHC – a été officiellement inauguré au congrès de l’EASL et de l’International Liver Congress (ILC). Grâce aux nouveaux antiviraux à action directe (AAD) et schémas oraux sans interféron administrés en 12 semaines seulement, l’hépatite C devient la première infection virale chronique que l’on puisse guérir à grande échelle. Les résultats de vastes essais internationaux de phase III sur de nouvelles bithérapies et trithérapies anti-VHC à dose fixe ont mis en évidence un taux de réponse virologique soutenue (RVS) (guérison) supérieur à 90 % chez des patients infectés par le VHC de génotype 1, le génotype prédominant en Amérique du Nord et en Europe. De plus, les mêmes résultats ont été obtenus chez des patients généralement difficiles à traiter comme des patients transplantés et des patients cirrhotiques. Peu de récidives ont été observées, et les taux d’abandons du traitement étaient faibles, ce qui témoigne de bons profils d’innocuité et de tolérabilité.
«Le congrès de 2014 fera date, car l’hépatite C est maintenant curable chez la quasi-totalité des patients», a déclaré la présidente d’honneur du congrès, la Pre Giorgina Mieli-Vergani (King’s College Hospital, Londres, Royaume-Uni), qui dirigeait la séance inaugurale. «Nous avons maintenant les outils voulus pour éliminer le virus de l’hépatite C [VHC]; c’est donc dire que nous sommes arrivés à bon port», affirmait le Pr Graham R. Foster, Queen Mary University of London, Royaume-Uni. Au Canada, tout comme en Europe de l’Ouest, notre objectif devrait être d’éliminer l’hépatite C, ce que – en étant optimistes – nous arriverons à faire en une dizaine d’années. Plus de 300 000 Canadiens sont aux prises avec une hépatite C chronique, mais moins de la moitié le savent. L’infection par le VHC – qui peut évoluer vers une cirrhose, une insuffisance hépatique et un carcinome hépatocellulaire – entraîne la perte d’un plus grand nombre d’années de vie et plus de morbidité que toute autre maladie infectieuse au Canada.
Schémas sans interféron
Le télaprévir et le bocéprévir, deux antiviraux à action directe (AAD) de première génération commercialisés en 2011, s’administrent avec la bithérapie interféron pégylé + ribavirine. Ils sont associés à un taux de réponse virologique soutenue (RVS) de 67 à 75 % chez des patients jamais traités auparavant (Jacobson IM et al. N Engl J Med 2011;364:2405-16; Poordad F et al. N Engl J Med 2011;364:1195-206) et de 29 à 38 % chez des patients dont la réponse antérieure à la bithérapie interféron pégylé + ribavirine avait été nulle (Zeuzem S et al. N Engl J Med 2011;364:2417-28; Vierling JM et al. J Hepatol 2014;60:748-56). Reposant sur l’interféron, ces premiers schémas entraînaient des effets indésirables (EI) importants qui avaient pour conséquence de limiter le traitement. Vers la fin de 2013, deux nouveaux AAD ont été homologués au Canada et dans d’autres pays : le sofosbuvir, inhibiteur nucléotidique de la polymérase NS5B, et le siméprévir, inhibiteur de la protéase, chacun étant actuellement indiqué en association avec la bithérapie interféron pégylé + ribavirine dans le traitement de l’infection par le VHC de génotype 1.
On a présenté au congrès de l’EASL des données de phase III sur deux nouveaux schémas oraux à base d’un AAD sans interféron qui ont été soumis aux autorités de nombreux pays pour homologation. Le premier – que l’on appelle «schéma 3D» – regroupe l’ABT-450/r, inhibiteur de la protéase NS3/4A potentialisé par le ritonavir, associé à l’ombitasvir (ABT-267), inhibiteur de la protéase NS5A (150 mg/100 mg/25 mg par jour), le dasabuvir (ABT-333), inhibiteur non nucléosidique de la protéase NS5B du VHC (250 mg 2 fois/jour), et la ribavirine (1000 à 1200 mg par jour). Le patient prend donc 3 comprimés matin et soir avec de la ribavirine. Le second schéma est une association à dose fixe regroupant le lédispavir (90 mg), inhibiteur de la protéase NS5A, et le sofosbuvir (400 mg) dans un comprimé unique que le patient prend 1 fois/jour avec ou sans ribavirine 2 fois/jour.
Patients jamais traités auparavant
À en juger par les résultats de SAPPHIRE-I, vaste essai de phase III mené avec randomisation et placebo à l’échelle internationale ayant pour objectif d’évaluer un schéma oral sans interféron chez des patients jamais traités pour une infection par le VHC de génotype 1, le schéma 3D est un traitement à la fois puissant, efficace et très bien toléré. Parmi les 473 patients (sur 631) randomisés de façon à recevoir le schéma 3D, 96 % sont parvenus à une RVS à 12 semaines (RVS12) (résumé 060; Feld JJ et al. N Engl J Med 2014;370:1594-603). Le taux de RVS12 – élevé sans égard au sous-type (1a ou 1b) du génotype du VHC (Figure 1) – excédait 90 % dans tous les sous-groupes, y compris ceux dont le taux de réponse avait toujours été faible. Sur le plan de la réponse, les chercheurs n’ont noté aucune différence entre les divers sous-groupes, à savoir : sexe, race, indice de masse corporelle, stade de la fibrose, taux initial d’ARN du VHC et dose de ribavirine.
Figure 1. SAPPHIRE-I, patients jamais traités : Taux de RVS12 selon le sous-type du génotype 1 du VHC
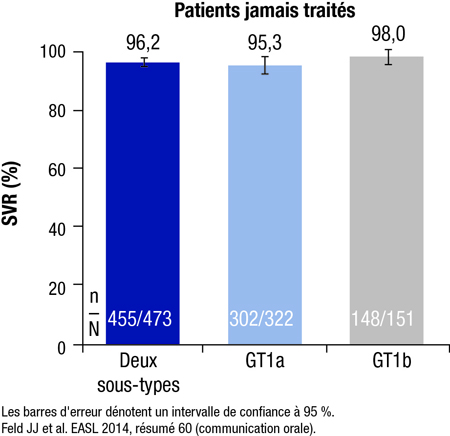
Le taux d’échecs virologiques était très faible : un seul échec sous traitement (0,2 %) et 7 récidives au décours du traitement (1,5 %). Tous ces patients avaient développé au moins une variante de la séquence d’acides aminés connue pour conférer une résistance à au moins un AAD du schéma et, selon toutes probabilités, à tous les AAD. Les chercheurs suivront ces patients afin de déterminer si les variantes persistent ou non. Tous les EI étaient d’intensité légère, tant dans le groupe de traitement actif que dans le groupe placebo, et la ribavirine a été généralement bien tolérée en l’absence d’interféron. Le taux d’EI signalés était plus élevé sous traitement actif, mais 73 % des patients sous placebo ont fait état de ≥1 effet indésirable. Il s’agit là d’un constat important, car il révèle que beaucoup d’EI ne sont probablement pas liés au traitement.
Selon les résultats d’un autre essai présentés au congrès – l’essai ION-1 – qui visait à évaluer l’association lédipasvir/sofosbuvir chez 865 patients jamais traités pour une infection par le VHC de génotype 1, aucun bénéfice supplémentaire n’est découlé de l’ajout de ribavirine ou d’une prolongation de la durée du traitement de 12 à 24 semaines (résumé O164; Afdhal N et al. N Engl J Med publié en ligne le 12 avril 2014). La Dre Alessandra Mangia, IRCCS Ospedale Casa Sollievo della Sofferenza, San Giovanni Rotondo, Italie, a fait mention de taux de RVS de 99 % et de 97 % avec ou sans ribavirine après 12 semaines et de 98 % et 99 %, respectivement, après 24 semaines de traitement. Aucune différence statistique n’a été mise en évidence entre les divers sous-groupes quant au taux de RVS. Seize patients ne sont pas parvenus à une RVS, et il y a eu 3 échecs virologiques (récidives dans tous les cas), mais aucun des facteurs cliniques examinés n’était prédictif de la récidive. Les EI et les valeurs de laboratoire anormales étaient principalement associés à la ribavirine, mais les taux d’abandons du traitement étaient plus élevés dans les groupes traités pendant 24 semaines, souligne la Dre Mangia.
L’essai ION-3, dont l’objectif était d’évaluer un traitement de plus courte durée, regroupait 647 patients non cirrhotiques randomisés de façon à recevoir l’association lédipasvir-sofosbuvir pendant 8 ou 12 semaines, avec ou sans ribavirine (résumé 066; Kowdley KV et al. N Engl J Med publié en ligne le 11 avril 2014). Le Dr Kris Kowdley, Virginia Mason Medical Center, University of Washington, Seattle, a pour sa part indiqué qu’il n’y avait aucune différence d’efficacité entre le schéma de 8 semaines et celui de 12 semaines (RVS 93%/94% avec/sans ribavirine après 8 semaines vs 95 % après 12 semaines sans ribavirine). Les récidives étaient plus fréquentes après 8 semaines de traitement qu’après 12 semaines (5 % vs 1 %). «Peut-être qu’un troisième antiviral serait approprié ou qu’une durée de traitement comprise entre 6 et 8 semaines serait possible, mais il faudra explorer ces possibilités, reconnaît le Dr Kowdley. À en juger par les résultats de l’essai ELECTRON, nous savons qu’une durée de 6 semaines n’est pas optimale avec ce schéma», note-t-il (Gane EJ et al. Gastroenterology 2014;146:736-43).
Patients porteurs d’un VHC de génotype 1b
Le Pr Peter Ferenci, École de médecine de Vienne, Autriche, a présenté des données «très claires» prouvant l’innocuité et l’efficacité du schéma 3D chez des patients porteurs du VHC de génotype 1b, le plus répandu des génotypes du VHC à l’échelle mondiale. Dans l’essai PEARL-III mené à double insu avec placebo, 419 patients jamais traités ont été randomisés de façon à recevoir le traitement avec ou sans ribavirine (résumé P1299). Après 12 semaines de traitement, 99 % des patients de chaque groupe étaient parvenus à une RVS. «Il faut surtout retenir qu’il n’est pas nécessaire d’administrer de la ribavirine aux patients non cirrhotiques infectés par le VHC de génotype 1b», explique le Pr Ferenci. Le taux de réponse était élevé dans tous les sous-groupes, y compris chez les patients dont les caractéristiques (sexe masculin, race noire, et génotype IL28B non-CC) ont toujours été associées à une réponse moindre au traitement. Aucun patient n’a abandonné le traitement en raison d’un EI, et aucun des patients recevant le schéma sans ribavirine n’a eu de récidive virologique ou d’échec en cours de traitement.
Patients déjà traités
Des patients (n=440) chez qui un traitement à base d’interféron pégylé, avec ou sans inhibiteur de la protéase, avait déjà échoué par le passé ont été recrutés dans l’essai ouvert ION-2 portant sur l’association lédipasvir/sofosbuvir avec ou sans ribavirine administrée pendant 12 ou 24 semaines (résumé 0109; Afdhal N et al. N Engl J Med 2014;370:1483-93). Le taux de RVS12 a été comparable dans tous les groupes (94 à 99 %), ce qui donne à penser que l’ajout de ribavirine et/ou la prolongation de la durée du traitement n’ont pas augmenté significativement le taux de RVS, précise le Dr Nezam Afdhal, Beth Israel Deaconess Medical Center, Harvard Medical School, Boston. Chez des patients cirrhotiques qui avaient déjà eu une réponse nulle, la prolongation du traitement à 24 semaines a été associée à un gain non significatif, mais le nombre de patients était restreint. Fait digne de mention, cet essai ciblait des patients chez qui un schéma à base d’un inhibiteur de la protéase de première génération (télaprévir/bocéprevir) avait échoué. Les taux de réponse ont été similaires, que les patients aient reçu auparavant la bithérapie interféron pégylé + ribavirin seule ou en association avec un inhibiteur de la protéase. Vu l’absence de chevauchement des profils de résistance du sofosbuvir et des inhibiteurs de la protéase, l’association lédipasvir/sofosbuvir avec ou sans ribavirine peut être utilisée à titre de traitement de sauvetage.
SAPPHIRE-II – vaste essai de phase III mené avec randomisation et placebo à l’échelle internationale pour l’évaluation d’un schéma sans interféron après un échec du traitement à base d’interféron pégylé – a mis en évidence un taux élevé de RVS12, comparable aux taux observés dans SAPPHIRE-I, précise le Pr Stefan Zeuzem, Université Johann Wolfgang Goethe, Francfort-sur-le-Main, Allemagne. L’essai SAPPHIRE-II regroupait 394 patients : 79 % des patients avaient déjà eu une récidive, 22 % avaient déjà répondu partiellement et 49 % avaient déjà été des répondeurs nuls (résumé O1; Zeuzem S et al. N Engl J Med 2014;370:1604-14). Le taux de RVS12 global – 96 % – demeurait inchangé, que le génotype du VHC ait été 1a ou 1b, qu’il y ait eu récidive ou non et que la réponse antérieure ait été nulle ou partielle. Ce sont là des «résultats incroyables», déclare le Pr Zeuzem (Figure 2). Aucun échec virologique n’a été enregistré au cours des 12 semaines de traitement. Sept récidives – la majorité chez des patients ayant déjà eu une réponse nulle à la bithérapie interféron pégylé + ribavirine – sont survenues entre la 2e et la 8e semaine suivant la fin du traitement. Le prurit, le plus fréquent des EI, était significativement plus fréquent sous traitement actif. Le taux d’abandons motivés par un EI était faible (1 %) et, parmi les EI graves (2,0 %), un seul a été considéré comme possiblement lié au schéma 3D. «Si j’en juge par notre expérience, c’est un traitement parfaitement bien toléré», confirme le Pr Zeuzem.
Figure 2. SAPPHIRE-II, patients déjà traités – Taux de RVS12 au sein de la population en intention de traiter, selon la réponse antérieure à la bithérapie interféron pégylé + ribavirine
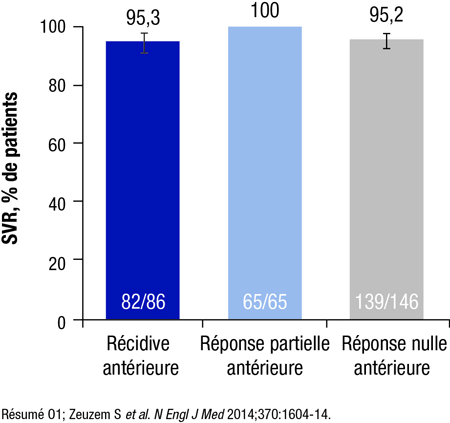
Populations difficiles à traiter
Le Dr Ed Gane de Nouvelle-Zélande a présenté des résultats de l’essai ELECTRON 2, dont l’objectif était d’évaluer l’association sofosbuvir/lédipasvir à dose fixe dans de petits groupes de patients difficiles à guérir. Dans le premier groupe, l’hépatite C avait récidivé après un traitement à base de sofosbuvir. Les 19 patients étaient parvenus à une RVS après 12 semaines de traitement en association avec ribavirine. Bien que cette étude ait été de petite envergure, elle a clairement montré que le seuil d’apparition d’une résistance au sofosbuvir était extrêmement élevé, les échecs tenant exclusivement aux récidives et non à l’apparition d’une résistance cliniquement significative. Il est très important de pouvoir traiter de nouveau le petit nombre de non-répondeurs. L’essai regroupait aussi 20 patients atteints d’une cirrhose de classe B de Child-Pugh qui ont reçu l’association à dose fixe pendant 12 semaines. Seulement 13 patients (65 %) sont parvenus à une RVS, mais ce nombre est une démonstration importante de l’innocuité et de l’efficacité éventuelle de ce schéma chez des patients dont la maladie hépatique est très avancée. On a observé une amélioration clinique chez ces patients et on fera un suivi afin de déterminer si le traitement prévient les complications à long terme ou en réduit le risque, surtout en ce qui a trait à la nécessité d’une transplantation hépatique.
Dans l’essai TURQUOISE-II, le premier essai visant à évaluer exclusivement un schéma oral sans interféron chez des patients atteints de cirrhose compensée, l’efficacité et l’innocuité du schéma 3D ont été comparables à ce que l’on avait observé chez des patients non cirrhotiques (résumé 0163; Poordad F et al. N Engl J Med publié en ligne le 12 avril 2014). L’essai mené en mode ouvert avec randomisation regroupait 380 patients atteints de cirrhose jamais traités ou déjà traités, ce qui en fait l’essai le plus vaste jamais réalisé au sein d’une population de patients cirrhotiques porteurs du VHC. Dans cette étude, les chercheurs avaient recruté des patients souvent considérés comme non admissibles aux essais cliniques, par exemple les patients présentant une thrombopénie marquée, une hypoalbuminémie et même une ascite visible à la radiographie. Après 12 ou 24 semaines d’administration du schéma 3D + ribavirine, 92 % et 96 % des patients, respectivement, sont parvenus à une RVS, «ce qui est un taux de réponse incroyable», déclare le Dr Fred Poordad, Texas Liver Institute-University of Texas Health Science Center, San Antonio (Figure 3).
Figure 3. TURQUOISE-II, patients ayant une cirrhose compensée – Taux de RVS après 12 et 24 semaines de traitement
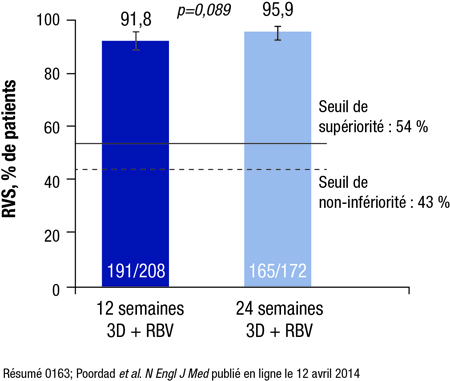
Le schéma a été bien toléré dans les deux groupes de traitement; en effet, peu d’effets indésirables (EI) graves et d’abandons du traitement ont été signalés. Un échec en cours de traitement a été observé chez un seul patient, mais il y a eu 12 récidives dans le groupe 12 semaines, ce qui porte le taux total d’échecs virologiques à 6 %, comparativement à 2 % dans le groupe 24 semaines. «C’est donc dire que certains de ces patients pourraient avoir intérêt à recevoir un traitement prolongé», estime le Dr Poordad. Le seul groupe dont les résultats semblaient d’autant meilleurs que le traitement durait longtemps était constitué de patients infectés par le génotype 1a qui avaient eu une réponse nulle à la bithérapie interféron pégylé + ribavirine.
Selon une étude de phase II menée chez des transplantés hépatiques aux prises avec des infections récurrentes par le VHC de génotype 1a ou 1b, le schéma 3D + ribavarine administré sur 24 semaines est associé à des taux de réponse élevés, explique le Dr Paul Kwo, Indiana University School of Medicine, Indianapolis. Au sein d’un groupe de 34 patients jamais traités après la transplantation, 100 % sont parvenus à une réponse virologique rapide, 100 % à une réponse en fin de traitement, 97 % à une RVS4 et 96 % à une RVS12 (résumé 0114). Le schéma a été bien toléré; les EI étaient généralement légers, et un seul patient a abandonné le traitement en raison d’EI. Aucun décès ni perte de greffon ni épisode de rejet aigu ou chronique n’a été signalé, et la posologie de l’inhibiteur de la calcineurine (tacrolimus ou cyclosporine) est demeurée acceptable durant la période de l’étude. «Avec de telles données, nous réussirons peut-être à retirer les transplantés hépatiques des populations particulières, tout comme nous semblons avoir retiré les patients infectés par le VIH à l’ère des AAD. Nous sommes impatients de connaître les résultats du suivi», déclare le Dr Kwo.
Résumé
Il est rare que les données présentées à un seul congrès aient des retombées aussi remarquables. Grâce à des traitements bien tolérés qui peuvent guérir la quasi-totalité des patients, y compris ceux dont la maladie hépatique est très avancée, nous pouvons aspirer pour la première fois à enrayer l’hépatite C au Canada. Les nouveaux médicaments constituent la première étape. Pour atteindre le noble objectif d’un Canada sans hépatite C, nous devrons investir dans les infrastructures du système de santé afin de dépister l’hépatite C au sein de la population, d’accroître le nombre de professionnels de la santé ayant eu la formation nécessaire pour traiter la maladie et d’améliorer l’accès aux soins pour tous ceux qui reçoivent un diagnostic d’hépatite C. Avec ces outils en place, nous serons en mesure d’obtenir d’aussi bons résultats dans la pratique que dans un cadre de recherche. Ces progrès arrivent à point nommé, car le Canada est sur le point de faire face à une augmentation importante des taux d’insuffisance et de cancer hépatiques, ce qui aura d’énormes répercussions sur l’économie et le système de santé si nous n’agissons pas rapidement. Fort heureusement, ces nouveaux traitements remarquables sont les outils dont nous avons besoin pour arriver à soulager le pays du lourd fardeau que représente l’hépatite C.