Comptes rendus
Faisons le point sur le SHUa : facteurs déclenchants, diagnostic et prise en charge
Le présent compte rendu est fondé sur des données médicales présentées lors d'un congrès de médecine reconnu ou publiées dans une revue avec comité de lecture ou dans un commentaire signé par un professionnel de la santé reconnu. La matière abordée dans ce compte rendu s'adresse uniquement aux professionnels de la santé reconnus du Canada.
PRESSE PRIORITAIRE - Semaine du rein 2022 – American Society of Nephrology (ASN)
En présentiel/virtuel, Orlando, Floride / 3-6 novembre 2022
En présentiel/virtuel – Le syndrome hémolytique et urémique atypique (SHUa) est une forme de microangiopathie thrombotique (MAT) qui touche principalement le rein, mais ses facteurs déclenchants et son tableau clinique varient énormément. Bien qu’il soit extrêmement rare, le SHUa a suscité beaucoup d’intérêt durant la Semaine du rein, la conférence phare de l’American Society of Nephrology (ASN). Au total, 19 communications par affiche et 4 résumés de publication ont porté sur divers aspects du SHUa. Des études de cas et de vastes analyses d’essais cliniques et du registre mondial du SHUa nous ont permis d’approfondir notre compréhension des facteurs déclenchants et du diagnostic du SHUa, et nous ont donné une nouvelle perspective sur l’issue clinique à long terme avec l’avènement des inhibiteurs du C5.
Rédactrice médicale en chef : Dre Léna Coïc, Montréal, Québec
« Le SHUa découle d’anomalies héréditaires ou acquises de la voie alterne du complément, et se caractérise par la triade classique anémie hémolytique avec Coombs négatif, thrombopénie et insuffisance rénale aiguë, mais d’autres organes peuvent être touchés », a expliqué le Dr Larry Greenbaum, Emory University School of Medicine, Atlanta, Géorgie, lorsqu’il a présenté son affiche. «Avant le développement de l’éculizumab, inhibiteur du C5, le pronostic du SHUa était sombre; insuffisance rénale terminale (IRT), morbidité et mortalité étaient monnaie courante1».
Dans une interview, le Dr Christoph Licht, SickKids Hospital, Toronto, Ontario, a discuté de notre compréhension actuelle de l’étiologie du SHUa. « Les maladies médiées par le complément ont généralement besoin de plus d’une “ frappe ” pour se développer; le patient doit avoir une prédisposition à la maladie, qu’il s’agisse d’une mutation génétique, de la présence d’anticorps ou d’un autre facteur que nous n’avons pas encore réussi à cerner, dit-il. Survient ensuite un événement inflammatoire ou infectieux qui intensifie l’activité du système du complément, et la maladie finit par apparaître. »
Regard sur les facteurs déclenchants du SHUa
Tentant d’explorer certaines de ces deuxièmes « frappes » ayant pu déclencher l’apparition d’un SHUa, le Dr Andrew Siedlecki, Brigham and Women’s Hospital, Boston, Massachussetts, et al. ont analysé les possibles facteurs déclenchants chez environ 1900 patients inclus dans le registre mondial du SHUa. Au total, 349 personnes ont été victimes d’un événement médical que l’on pourrait considérer comme un facteur déclenchant du SHUa, notamment : cancer, infection aiguë, maladie autoimmune, greffe du rein, hypertension maligne, apparition à la naissance, infection chronique, traitement médicamenteux, greffe de moelle osseuse, et glomérulopathie à dépôt de C3. Chez les adultes, le facteur déclenchant le plus fréquent était un cancer (22 %); chez les enfants, c’était une infection aiguë (36 %). Le moment de l’apparition de la maladie dépendait du facteur déclenchant. Les SHUa déclenchés par une infection aiguë, une hypertension maligne ou une greffe du rein apparaissaient généralement en l’espace de quelques jours à une semaine, alors que pour les SHUa déclenchés par une infection chronique, un traitement médicamenteux ou une maladie autoimmune, le délai entre le facteur déclenchant et la maladie cliniquement manifeste pouvait atteindre deux à trois ans2.
Le Dr Licht, collaborateur du registre et président sortant du comité scientifique consultatif, y est allé de quelques conseils complémentaires à la lumière de ces résultats. « Au vu des différents facteurs déclenchants, il est important de comprendre la fenêtre de risque afin de mettre ces enseignements en pratique, poursuit-il. Les infections étant généralement des phénomènes transitoires de courte durée, le scénario est alors plus simple; par contre, si le facteur déclenchant est un cancer, il ne disparaîtra pas en 3 semaines! En pareils cas, il est important d’éduquer le patient – ou les parents de l’enfant – quant aux signes d’une éventuelle réémergence de la maladie à surveiller à l’arrêt du traitement médicamenteux. »
Difficultés du diagnostic et outils potentiels dans le SHUa
« Bien que le SHUa soit une forme rare de MAT, nous devons le considérer comme une urgence médicale et, de ce fait, le diagnostic précoce est essentiel », affirmait le Dr Miguel Uriol Rivera, Hospital universitario Son Espases, Palma de Majorque, Espagne, dans une interview par courriel. Il est parfois difficile de différencier un SHUa des autres types de MAT en raison de sa physiopathologie complexe et des longs délais d’obtention des résultats des tests génétiques. L’une des difficultés du diagnostic différentiel est de distinguer le SHUa des autres formes de MAT, en particulier le purpura thrombotique thrombopénique (PTT). Le score PLASMIC a été conçu et validé en tant qu’outil diagnostique pour un PTT; un score de 6 ou plus sur cette échelle en 7 points témoigne d’un PTT probable3. Dans l’affiche qu’ils ont présentée à la Semaine du rein, le Dr Uriol Rivera et al. ont tenté de déterminer s’il pouvait aussi être utile pour le diagnostic d’un SHUa en analysant des cas confirmés de SHUa dans le cadre d’essais sur l’éculizumab et le ravulizumab, deux inhibiteurs du C5. « Notre étude a révélé que 87 % des patients présentaient un score PLASMIC inférieur à 6, associé à une numération plaquettaire supérieure à 30 000/μL et à une légère détérioration de la fonction rénale (créatinine plasmatique > 2 mg/dL) », poursuit le Dr Uriol Rivera (Figure 1). « Dans la pratique clinique, en cas d’indice élevé de suspicion clinique, l’utilisation du score PLASMIC et la recherche de ces caractéristiques pourraient accélérer le processus diagnostique4. »
Figure 1.
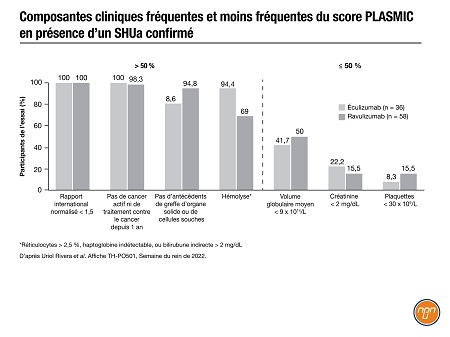
La prochaine étape sera de valider le score PLASMIC dans de plus vastes registres de MAT et des études prospectives, enchaîne le Dr Uriol Rivera. « De plus, si le score PLASMIC représente une approche pronostique qui facilite le choix du meilleur traitement, ce serait un outil précieux non seulement dans l’intérêt du patient, mais aussi du système de santé », conclut-il.
Issue clinique du traitement d’un SHUa
Depuis sa commercialisation en 2011, l’éculizumab, inhibiteur du C5 devenu le traitement de référence du SHUa au Canada, a eu un impact énorme sur la morbidité et la mortalité. Juste avant la Semaine du rein, le ravulizumab, dérivé de l’éculizumab qui s’administre à intervalles plus longs, a été homologué au Canada : il devient donc la deuxième option pour le traitement ciblé du SHUa chez les adultes et les enfants de 1 mois ou plus. Plusieurs analyses présentées au congrès ont porté sur l’issue à long terme du SHUa et les pratiques exemplaires dans le traitement dirigé contre le complément.
Dans une communication par affiche, le Dr Greenbaum et al. se sont penchés sur les résultats à long terme consignés dans le registre mondial sur le SHUa chez des patients qui avaient reçu l’éculizumab pendant au moins 90 jours. Durant le suivi de trois ans, les patients de la cohorte A (n = 249) n’ont pas présenté d’insuffisance rénale terminale (IRT); chez les patients de la cohorte B (n=56), le SHUa a évolué vers une IRT peu de temps après le début du traitement par l’éculizumab. Dans les deux cohortes, les chercheurs ont observé une amélioration marquée des paramètres hématologiques depuis le début du traitement jusqu’au dernier suivi et, dans le cohorte A, le débit de filtration glomérulaire estimé (DFGe) s’est aussi amélioré. Le taux de mortalité a été plus élevé dans la cohorte B (14,3 %) que dans la cohorte A (0,8 %). Bien qu’il n’y ait pas de lien évident entre les caractéristiques initiales des patients et la réponse au traitement ou l’évolution vers une IRT, les résultats dans leur ensemble étayent les effets favorables à long terme de l’éculizumab sur les paramètres hématologiques et rénaux chez une proportion importante de patients1.
Dans le traitement du SHUa, la durée du traitement par l’éculizumab est une grande inconnue : faut-il le poursuivre indéfiniment ou serait-il approprié dans certains cas de l’interrompre après le premier cycle et de surveiller un éventuel retour de la maladie? Dans une communication par affiche, la Dre Romy Bouwmeester, Centre médical de l’Université de Radboud, Pays-Bas, et al. ont présenté les résultats d’une étude observationnelle prospective de 4 ans sur le SHUa (CUREiHUS) chez des patients non transplantés qui avaient reçu de l’éculizumab pendant 3 mois. Après l’arrêt du traitement, une rechute clinique est survenue chez seulement 22 % (n = 4) des patients, même si la majorité (81 %) des patients présentaient un variant génétique connu du complément ou des anticorps qui pouvaient déterminer leur prédisposition au SHUa. Les patients qui ont rechuté ont de nouveau reçu un traitement par l’éculizumab et n’ont pas eu de séquelles à long terme. L’interruption du traitement a réduit le coût global des soins de santé d’environ 70 % comparativement au traitement sans interruption. « Il est sûr et efficient d’interrompre le traitement par l’éculizumab après 3 mois chez les patients atteints d’un SHUa qui n’ont pas eu de greffe rénale5 », concluent les auteurs.
Conclusions
Maintenant que les grands registres et les essais cliniques nous pernettent d’analyser de plus vastes cohortes de patients, nous pouvons confirmer à la lumière de ces cas et de notre expérience clinique ce que nous comprenons de la physiopathologie du SHUa et de son issue clinique, et bâtir sur ces acquis. De nouveaux outils diagnostiques comme le score PLASMIC pourraient être utiles pour accélérer le diagnostic et l’instauration du traitement. L’inhibition du complément demeure le traitement de référence du SHUa, car cette approche diminue la mortalité et améliore l’issue hématologique et rénale à long terme; chez les patients appropriés, un traitement de durée limitée pourrait nous permettre de réaliser des économies tout en demeurant efficace.
Références :
1. Greenbaum LA et al. Affiche TH-PO502 présentée à la Semaine du rein, 3–6 nov. 2022.
2. Siedlecki A et al. Affiche TH-PO500 ibid.
3. Li A et al. J Thromb Hemost. 2018; 16: 164–169.
4. Uriol Rivera MGet al. Affiche TH-PO501 présentée à la Semaine du rein, 3–6 nov. 2022.
5. Bouwmeester RN et al. Affiche TH-PO503 ibid.